灵迪说明书
Cefepime Hydrochloride for Injection
头孢吡肟
本品的主要成份为盐酸头孢吡肟。
化学名称:氯化 1-[[(6R,7R)-7-[(2Z)-(2-氨基噻唑-4-基)-2-(甲氧亚氨基)乙酰氨基]-2-羧基-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-3-基]甲基]-1-甲基吡咯烷-盐酸盐-水合物。
化学结构式:
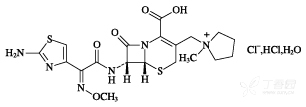
分子式 C19H25ClN6O5S2·HCl·H2O
分子量 571.50
辅料名称:L-精氨酸
本品为白色至微黄色粉末。
本品可用于治疗成人和 2 月龄至 16 岁儿童下述敏感细菌引起的中重度感染,包括下呼吸道感染(肺炎和支气管炎),单纯性下尿路感染和复杂性尿路感染(包括肾盂肾炎),非复杂性皮肤和皮肤软组织感染,复杂性腹腔内感染(包括腹膜炎和胆道感染),妇产科感染,败血症,以及中性粒细胞减少伴发热患者的经验治疗。 也可用于儿童细菌性脑脊髓膜炎。
怀疑有细菌感染时应进行细菌培养和药敏试验,但是因为头孢吡肟是一革兰阳性和革兰阴性菌的广谱杀菌剂,故在药敏试验结果揭晓前可开始头孢吡肟单药治疗。对疑有厌氧菌混合感染时,建议合用其他抗厌氧菌药物,如甲硝唑进行初始治疗。一旦细菌培养和药敏试验结果揭晓,应及时调整治疗方案。
本品可用静脉滴注或深部肌内注射给药。
成人和 16 岁以上儿童或体重为 40 公斤或 40 公斤以上儿童患者,可根据病情,每次 1~2 克,每 12 小时一次,静脉滴注,疗程 7~10 天;轻中度尿路感染,每次 0.5~1 克,每 12 小时一次,静脉滴注或深部肌内注射,疗程 7~10 天;重度尿路感染,每次 2 克,每 12 小时一次,静脉滴注,疗程 10 天;对于严重感染并危及生命时,可以每 8 小时 2 克静脉滴注;用于中性粒细胞减少伴发热的经验治疗,每次 2 克,每 8 小时一次静脉滴注,疗程 7~10 天或至中性粒细胞减少缓解。如发热缓解但中性粒细胞仍处于异常低水平,应重新评价有无继续使用抗生素治疗的必要。
2 月龄至 12 岁儿童,最大剂量不可超过成人剂量(即每次 2 克剂量)。体重超过 40 公斤的儿童的剂量,可使用成人剂量。一般可每公斤体重 40 毫克,每 12 小时静脉滴注,疗程 7~14 天;对细菌性脑脊髓膜炎儿童患者,可为每公斤体重 50 毫克,每 8 小时一次,静脉滴注。对儿童中性粒细胞减少伴发热经验治疗的常用剂量为每公斤体重 50 毫克,每 12 小时一次(中性粒细胞减少伴发热的治疗为每 8 小时一次),疗程与成人相同。
2 月龄以下儿童经验有限。可使用每公斤体重 50 毫克剂量。然而 2 月龄以上儿童患者的资料表明,每公斤 30 毫克,每 8 或 12 小时一次对于 1 至 2 月龄儿童患者已经足够。对 2 月龄以下儿童使用本品应谨慎。
儿童深部肌内注射的经验有限。
对肝功能不全患者,无调节本品剂量的必要。
对肾功能不全病人,如肌酐清除率低于(含)60 ml/min,则应调节本品用量,弥补这些病人减慢的肾清除速率。这些病人使用头孢吡肟的初始剂量与肾功能正常的患者相同,维持剂量和给药间隙时间如下:

头孢吡肟治疗同时需进行血液透析的患者,在透析开始 3 小时,约 68% 药物可被清除。血液透析患者的马斯平剂量见上表。接受持续性腹膜透析患者应每隔 48 小时给予常规剂量。
尚无肾功能不全的儿童患者使用头孢吡肟的资料。但是,因为成人和儿童的头孢吡肟药代动力学相似,肾功能不全儿童患者头孢吡肟的用法与成人类似。
静脉给药: 对于严重或危及生命的病例,应首选静脉给药。
静脉滴注时,可将本品 1~2 克溶于 50~100 毫升 0.9% 氯化钠注射液,5% 或 10% 葡萄糖注射液,M/6 乳酸钠注射液,5% 葡萄糖和 0.9% 氯化钠混合注射液,乳酸林格氏和 5% 葡萄糖混合注射液中,药物浓度不应超过每毫升 40 毫克。经约 30 分钟滴注完毕。
肌内注射: 肌内注射时,本品 0.5 克应加 1.5 毫升注射用溶液,或 1 克加 3.0 毫升溶解后,经深部肌群(如臀肌群或外侧股四头肌)注射。
本品禁用于对头孢吡肟或 L-精氨酸,头孢菌素类药物,青霉素或其他β-内酰胺类抗菌素有即刻过敏反应的病人。
本品禁用于对头孢吡肟或L—精氨酸,头孢菌素类药物,青霉素或其他β—内酰胺类抗生素有即刻过敏反应的病人请将药品存放在儿童触摸不到的地方。
请将药品存放在儿童触摸不到的地方。
使用本品前, 应该确定患者是否有头孢吡肟、其他头孢菌素类药物, 青霉素或其他β-内酰胺类抗菌素过敏史。对于任何有过敏, 特别是药物过敏史的患者应谨慎。
广谱抗菌药可诱发伪膜性肠炎。在用本品治疗期间患者出现腹泻时应考虑伪膜性肠炎发生的可能性。对轻度肠炎病例,仅停用药物即可;中、重度病例需进行特殊治疗。有胃肠道疾患,尤其是肠炎患者应谨慎处方头孢吡肟。
与其他头孢菌素类抗生素类似,头孢吡肟可能会引起凝血酶原活性下降。对于存在引起凝血酶原活性下降危险因素的患者,如肝、肾功能不全,营养不良以及延长抗菌治疗的患者应监测凝血酶原时间,必要时给予外源性维生素 K。
本品所含精氨酸在所用剂量为最大推荐剂量的 33 倍时会引起葡萄糖代谢紊乱和一过性血钾升高。较低剂量时精氨酸的影响尚不明确。
对肾功能不全(肌酐清除率 ≤ 60 ml/min)的患者,应根据肾功能调整本品剂量或给药间歇时间。
本品与氨基糖苷类药物或强效利尿剂合用时,应加强临床观察,并监测肾功能,避免引发氨基糖苷类药物的肾毒性或耳毒性作用。
用药过量患者,应仔细观察并使用支持疗法,并用血液透析治疗促进药物的排除,而不宜采用腹膜透析。在血透开始的3小时内,体内68%的头孢吡肟可排出。
虽然动物生殖毒性试验和致畸试验表明头孢吡肟无致畸和胚胎毒性,但尚无本品用于孕妇和分娩时妇女的足够和有良好对照的临床资料。所以,本品用于孕妇应谨慎。 头孢吡肟在人乳汁中有极少量排出(浓度约 0.5 μg/ml)。头孢吡肟用于哺乳期妇女应谨慎。肾功能正常的老年患者使用一般推荐剂量,其疗效和安全性与其他成年患者相似;肾功能不全老年患者使用本品,应根据肾功能调整给药计划。2月龄至12岁儿童,最大剂量不可超过成人剂量(即每次2克剂量)。体重超过40公斤的儿童的剂量,可使用成人剂量。一般可每公斤体重40毫克,每12小时静脉滴注,疗程7-14天;对细菌性脑脊髓膜炎儿童患者,可为每公斤体重50毫克,每8小时一次,静脉滴注。对儿童中性粒细胞减少伴发热经验治疗的常用剂量为每公斤体重50毫克,每12小时一次(中性粒细胞减少伴发热的治疗为每8小时一次),疗程与成人相同。 2月龄以下儿童经验有限。可使用每公斤体重50毫克剂量。然而2月龄以上儿童患者的资料表明,每公斤30毫克,每8或12小时一次对于1至2月龄儿童患者已经足够。对2月龄以下儿童使用本品应谨慎。 儿童深部肌肉注射的经验有限。
B级:
和多数β-内酰胺抗生素一样,由于药物的相互作用,头孢吡肟溶液不可加至甲硝唑,万古霉素,庆大霉素,妥布霉素或硫酸奈替米星,氨茶碱溶液中。 头孢吡肟浓度超过40mg/ml时,不可加至氨苄青霉素溶液中。如有与头孢吡肟合用的指征,这些抗菌素应与头孢吡肟分开使用。 头孢吡肟可引起尿糖试验假阳性反应。建议使用本品治疗期间,使用葡萄糖氧化酶反应检测方法。
海南海灵化学制药有限公司
86905776000066
头孢吡肟为广谱第四代头孢菌素,通过抑制细菌细胞璧的生物合成而达到杀菌作用。体外试验表明,本品对革兰阳性菌和阴性菌均有作用。本品对细菌染色体编码的β-内酰胺酶亲和力低,可高度耐受多数β-内酰胺酶的水解,并可迅速渗入革兰阴性菌的细胞内。在菌体细胞内,其靶分子为青霉素结合蛋白(PBP)。
体外和临床感染研究证实本品对以下大多数微生物有活性。
革兰阴性需氧微生物:
肠杆菌属、肺炎克雷伯杆菌、大肠杆菌、奇异变形杆菌、绿脓杆菌。
革兰阳性需氧微生物:
金黄色葡萄球菌(仅针对甲氧西林敏感的菌株)、化脓性链球菌(A 组链球菌)、肺炎链球菌。
本品体外对以下大多数微生物有活性,但是尚无充分和严格的临床感染性疾病治疗的支持。
革兰阴性需氧微生物:
醋酸钙不动杆菌、弗氏枸橼酸菌、异型枸橼酸菌、聚团肠杆菌属、流感嗜血杆菌(包括产β-内酰胺酶菌株)、蜂房哈夫尼菌、奥克西托克雷伯杆菌、莫拉卡他菌(包括产β-内酰胺酶菌株)、普通变形杆菌、雷氏变形杆菌、斯氏普罗维登斯菌、粘质沙雷菌。
本品对多数寡养单胞菌株无活性。
革兰阳性需氧微生物:
表皮葡萄球菌(仅针对甲氧西林敏感的菌株)、腐生性葡萄球菌、无乳链球菌(B 组链球菌)。
多数肠球菌,如粪肠球菌和耐甲氧西林葡萄球菌对本品耐药。
厌氧微生物:
革兰阴性杆菌(包括脆弱拟杆菌、其他拟杆菌属和梭杆菌属)、革兰阳性和革兰阴性球菌(包括消化球菌、消化链球菌和韦荣氏球菌属)、革兰阳性杆菌(包括梭状芽孢杆菌、真杆菌和乳杆菌属)。
遗传毒性:体内、外的研究结果均未发现本品有遗传毒性。
生殖毒性:小鼠、大鼠和兔分别给予本品剂量为 1200、1000、100 mg/kg(以体表面积计,分别相当于临床推荐人用最大剂量的 1-4 倍),均未见本品对动物生育力和生殖有明显影响。但是尚无充分和严格的孕妇研究资料,动物与人的相关性尚不清楚。
给药方法:
试验药与对照药均为 2 g/次,2 次/日,加入 100 ml 生理盐水中,60-90 min 匀速静脉滴注。
研究对象:
1.年龄 18-65 岁的住院或门诊患者(慢性支气管炎急性发作部分患者年龄可放宽至 70 岁)。
2.经临床确诊为细菌感染需进行全身抗生素治疗的患者(以中重度感染为主)。
3.通过细菌学检查,80% 以上的受试者细菌培养需阳性,少部分细菌培养阴性的受试者,必须有细菌感染的临床症状、体征及相应的实验室检查结果。
4.受试者试验前未用过其他抗生素治疗,或经其他抗生素治疗无效而细菌学检查为阳性并单独用此药治疗者。
5.受试者需签署知情同意书。
主要观察指标:
(1)临床观察:用药前、用药期间、治疗结束后,每日详细观察患者临床表现并做体检,包括临床症状、体征。症状、体征严重程度以轻度、中度、重度表示。并将检查结果填入病例登记表。
(2)实验室检查
1.血常规(包括 Hb、RBC、WBC + DC、PLT):治疗前、停药后第 1 天必须进行。如治疗前检查异常,应于给药第 4 天复查;停药后第 1 天检查如为异常,可于停药 1 周后复查。
2.尿常规(包括 pH、蛋白、糖、酮体、WBC、RBC):治疗前、停药后第 1 天必须进行,如治疗前检查异常,应于给药第 4 天复查:停药后第 1 天检查如为异常,可于停药 1 周后复查。
3.血生化检查(包括 ALT、AST、ALP、TBIL、DBIL、UREA、Cr)治疗前、停药后第 1 天必须进行;如果停药第 1 天检查异常,应于停药后 1 周复查。
以上异常结果需随访至正常。
4.尿妊娠试验:育龄妇女,未采取绝育措施者,入选前须进行尿妊娠试验,试验阴性者方能入选。
临床试验的结果:
本研究以注射用盐酸头孢吡肟为试验药,注射用头孢他啶为对照药进行随机对照试验,治疗急性呼吸系统和泌尿系统细菌性感染 120 例,取得了满意的临床疗效。临床研究试验结果显示:试验组和对照组细菌培养阳性率分别为 88.1% 和 78.7%,两组痊愈率分别为 67.80% 和 73.77%,有效率分别为 100% 和 93.44%(PPT 分析)。两组单菌种和单病种的临床疗效比较均无显著性差异(P>0.05)。两组细菌学效果比较无显著性差异(P>0.05)。我们将所得到的细菌进行体外抗菌活性测定,结果显示:除加替沙星,头孢噻肟外,头孢哌酮/舒巴坦、头孢他啶的敏感率与头孢吡肟比较均无显著性差异(P>0.05)。
本次试验表明,注射用盐酸头孢吡肟与注射用头孢他啶一样具有良好的耐受性。试验组出现 5 例不良事件,表现为 3 例血中白细胞下降,1 例头晕,很可能与药物有关,1 例皮疹,与药物肯定有关。对照组出现 5 例不良事件,3 例表现为血中白细胞下降,1 例血白细胞、红细胞、血红蛋白下降,很可能与药物有关,1 例头痛,与药物可能有关。两组不良事件和不良反应发生率比较没有显著性差异(P>0.05)。
本品 0.25 克~2 克静脉单剂量输注,呈线性药代动力学,头孢吡肟的平均血浆消除半衰期为 2.0±0.3 小时,机体总清除率为 120.0±8.0 毫升/分钟。肌内给药,头孢吡肟可完全被吸收,血药浓度达峰时间(tmax)约为 1.5 小时,在 0.5 克~2.0 克剂量范围内,药代动力学呈线性。健康成年男性志愿者接受临床剂量的头孢吡肟连续 9 天,未见积蓄。
头孢吡肟与血清蛋白的结合率约为 20%,且与药物血浓度无关。头孢吡肟平均稳态分布容积为 18.0±2.0 升,在尿液、胆汁、腹膜液、水泡液、气管粘膜、痰液、前列腺液、阑尾、胆囊中均能达到治疗浓度,并可通过炎性血脑屏障。
头孢吡肟主要经肾分泌排出。在体内有少量亦可经转化为 N-甲基吡咯烷(NMP)最后代谢为 N-甲基吡咯烷氧化物(NMP-N-氧化物)。头孢吡肟和其代谢产物主要经肾排泄,尿液中头孢吡肟原形为摄入量的 85%,NMP 不足 1%,NMP 氧化物约为 6.8%,头孢吡肟异构体约为 2.5%。
亦有少量头孢吡肟可自人体乳腺分泌排出。
2 月龄至 11 岁单剂静脉注射头孢吡肟,机体总清除率和稳态分布容积分别为 3.3±1.0 毫升/分钟/公斤体重和 0.3±0.1 升/公斤体重,尿液中头孢吡肟原形为给药量的 60.4±30.4%,平均肾清除率为 2.0±1.1 毫升/分钟/公斤体重。按体重校正,药物清除率和分布容积在儿童性别和年龄间无差异。50 毫克/公斤体重,12 小时一次给药,未见药物蓄积,而每 8 小时一次给药,稳态时的 Cmax、AUC 和半衰期约增加 15%。儿童 50 毫克/公斤体重静脉注射的 AUC 与成人 2 克静脉给药的暴露量相当。肌内注射的绝对生物利用度为 82.3±15%。
65 岁和 65 岁以上的老年人给予头孢吡肟,药物总清除率下降。
肾功能不全患者中头孢吡肟的总清除率与肾肌酐清除率相关。需接受血透的患者中,头孢吡肟的平均消除半衰期为 13.5±2.7 小时,需持续腹膜透析的患者中,半衰期为 19.0±2.0 小时。因此,肾功能不全患者使用本品应注意调整剂量或/和给药间期。 肝功能不全头孢吡肟药代动力学无改变,这些病人无需调整剂量。
注射剂
1.0g(按C19H24N6O5S2计算)
注射用玻璃瓶装,1瓶/盒。
遮光、密闭、在干燥凉暗处(不超过20℃)保存。
8.00元起
暂定18个月
J01DE01-头孢吡肟
国药准字H20061074
国家基本药物目录;国家基本医疗保险和工伤保险药品


