卡全说明书
Fat Emulsion,Amino Acids (17) and Glucose (19%) Injection
葡萄糖
本品的包装袋为内袋与外袋,在内袋与外袋之间防止吸氧剂,内袋有二条可撕裂封条分隔成 3 个独立的腔室,分别装有葡萄糖注射液,氨基酸注射液及脂肪乳注射液。
本品有四种包装规格,每种规格所含葡萄糖、氨基酸及脂肪乳注射液体积见下表:
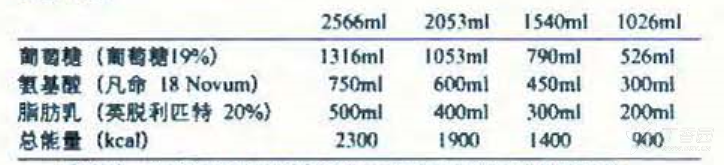
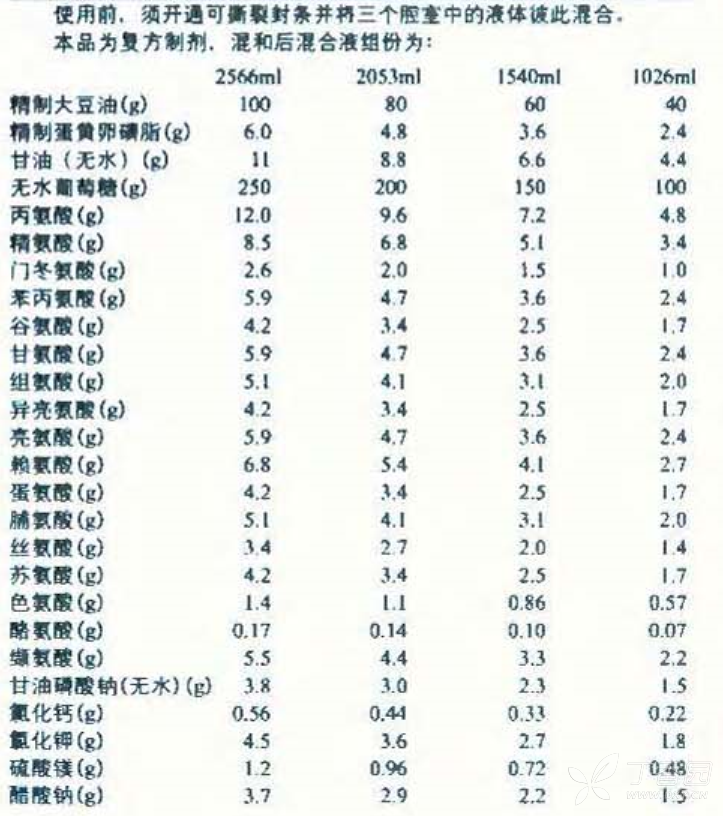
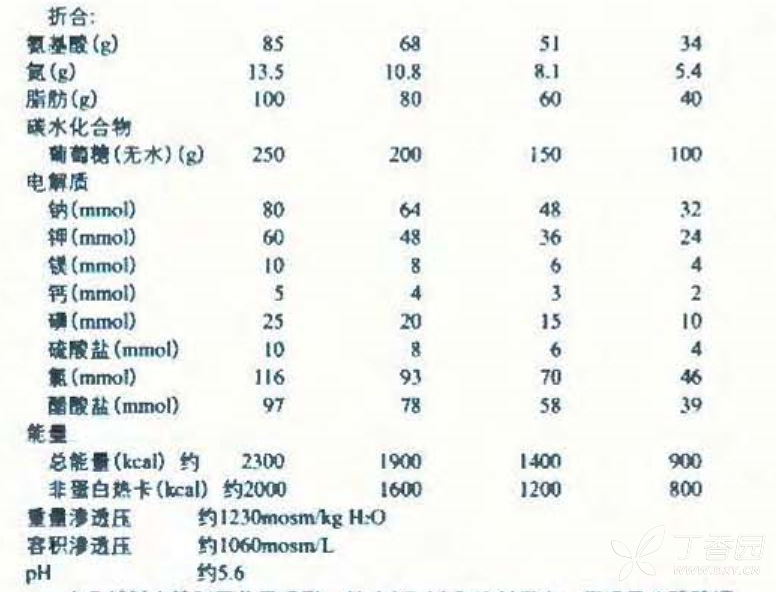
本品辅料为精致蛋白卵磷脂、甘油(无水)和注射用水、用适量冰醋酸调节氨基酸注射液 PH,适量氢氧化钠调节脂肪乳注射液 PH。
脂肪乳注射液为白色乳状液体,复方氨基酸注射液为无色或微黄色的澄明液体,葡萄糖注射液为无色或几乎无色的澄明液体。三腔袋的混合溶液为白色乳状液体。
本品用于不能或功能不全或被禁忌经口/肠道摄取营养的成人患者。
本品仅推荐经中心静脉进行输注。
根据患者临床情况、体重以及营养需求选择不同规格的本品。为满足患者全部的营养需求,应考虑添加微量元素以及维生素。
维持机体氮平衡所需的氮量应根据患者实际情况(如营养状况与代谢应激等)决定。一般营养状况或轻度代谢应激的患者,其氮的需要量为按体重一日0.10~0.15g/kg;有中度或重度代谢应激(无论有无营养不良)的患者,其氮需要量为按体重为一日0.15~0.30g/kg(相当于氨基酸量一日1.0~2.0g/kg)。而葡萄糖与脂肪一般推荐需要量分别为按体重一日2.0~6.0g/kg与1.0~2.0g/kg。
输注速率:按患者体重葡萄糖最大输注速率为一小时0.25g/kg,氨基酸输注速率不宜超过一小时0.1g/kg,脂肪则不超过一小时0.15g/kg。
本品输注速率按患者体重不宜超过一小时2.6ml/kg(相当于0.25g葡萄糖、0.09g氨基酸、0.1g脂肪/kg)。推荐输注时间为12~24小时。
本品使用时间长短由患者临床营养状况而定。
使用前需将三腔内液体互相混合。当打开可撕裂封条、三腔内液体互相混合后,在25℃下其物理与化学性质能稳定24小时。
使用方法图示见后。


与所有高渗性输液一样,如采用周围静脉输注有可能发生静脉炎。
输注英脱利匹特(脂肪乳注射液)可能会引起体温升高(发生率<3%),偶见寒战、恶心/呕吐(发生率<1%)。另有静脉营养过程中出现一过性肝功能酶升高的报道。
因输注英脱利匹特产生其它不良反应可能性更小(小于每百万分之一)。超敏反应(过敏反应、皮疹、荨麻疹)与呼吸症状(呼吸急促)以及高/低血压等曾有报道;溶血、网织红细胞增多、腹痛、头痛、疲倦、阴茎异常勃起也曾有报道。
脂肪超载综合症:
脂肪廓清受损后会出现脂肪超载综合症,脂肪超载综合症也会出现在虽以推荐剂量速率输注、但由于临床情况突然发生改变的患者(如肾功能损伤与感染)。
脂肪超载综合症表现有高脂血症,发热,脂肪浸润,肝肿大,脾肿大,贫血,白细胞减少症,血小板减少症、凝血机制障碍,昏迷。若停止输注所有症状通常均可逆转。
对鸡蛋或大豆蛋白或处方中任一成份过敏者
重度高脂血症
严重肝功能不全
严重凝血机制障碍
先天性氨基酸代谢异常
严重肾功能不全且无法进行腹透与血透者
急性休克
高糖血症(胰岛素治疗超过6单位/小时)
血电解质(指本品处方中所含有的)水平出现异常升高
其它一般禁忌(如急性肺水肿,水潴留,失代偿性心功能不全,低渗性脱水)
吞噬血细胞综合症
疾病状态处于非稳定期(如严重创伤后期,失代偿性糖尿病,急性心梗,代谢性酸中毒,严重败血症,高渗性昏迷等)
须经常检测脂肪廓清能力。推荐检测方法是在输注结束5~6小时后进行。输注期间血清甘油三酯不宜超过3mmol/L。
水、电解质代谢紊乱(如异常高或低的血清电解质水平)的患者在使用本品前须对有关指标予以纠正。
开始输注本品前应特别谨慎小心。由于采用中心静脉输注会增加感染的机会,所以一旦出现任何异常现象,应立即停止输注。同样在静脉插管与操作观察中,应严格执行无菌操作。
对脂质代谢受损----如肾功能不全、失代偿性糖尿病、胰腺炎、肝功能损害、甲状腺功能低下(伴有高脂血症)以及败血症患者,应谨慎使用本品。如需使用则应密切观察血清甘油三酯浓度。
另外,应监测血糖、血电解质、血浆渗透压、水电解质平衡与酸碱平衡、以及肝功能酶(如碱性磷酸酶、ALT、AST)的情况。
长期进行脂肪输注时,还应检测血细胞计数与凝血状况。
当患者伴有肾功能不全则应密切监测磷与钾的摄入以防产生高磷血症与高钾血症。
根据患者电解质实际水平,可另补充电解质,但应密切监测血电解质变化情况。
对代谢性酸中毒、乳酸酸中毒、细胞供氧不足、血浆渗透压增高的患者应谨慎给予肠外营养。
对有电解质潴留的患者,应谨慎使用本品。
出现过敏性反应(如发热、寒战、皮疹、呼吸困难)的患者应立即停止输注。
由于本品含有脂肪,故在血清脂肪被廓清之前采血监测可能会出现干扰某些实验室指标现象(如胆红素、乳酸脱氢酶、氧饱和度、血红蛋白)。对大多数患者而言,血清脂肪廓清时间为5~6小时。
静脉输注氨基酸往往伴随尿铜尿锌排出的增加,因此对静脉营养(尤其是长期静脉营养)的患者应注意微量元素的补充。
对营养不良患者开始进行营养支持有可能会诱发肺水肿、充血性心力衰竭,同时还可能出现血钾、血磷、血镁以及血中水溶性维生素浓度的降低,上述改变可以在24~48小时内发生,因此开始给予静脉营养应格外小心,并密切观察并调整液体、电解质、矿物质与维生素的用量。
鉴于假性凝集作用,禁止本品与输血/血制品同用一根(套)输液管(器)。
如患者出现高糖血症需另外补充胰岛素。
只有在氨基酸溶液与葡萄糖溶液澄清且无色/微黄、脂肪乳溶液呈白色均质状态方可使用本品,使用前需将本品充分混匀。
当以超过最大推荐输注速率输注时可能会出现恶心、呕吐与出汗症状。如出现过量使用症状则减慢输注速率或停止输注。 另外过量使用会导致液体负荷加重、电解质紊乱、高血糖、血渗透压升高。 极少数严重患者可能需要血液透析,血液过滤。
尚不明确。尚不明确。本品不适宜新生儿与2岁以下婴幼儿使用。 本品是为成人患者设计,儿童蛋白质与能量的单位体重需要量可能会大于【用法用量】项下所列的成人的需要量。本品可用于老年患者。 老年患者蛋白质与能量的单位体重需要量可能会小于【用法用量】项下所列的成人的需要量。或遵医嘱。
只有在相容性得到证实的前提下,且所有的添加操作在严格无菌条件下,其它治疗药物或营养药物方可加入到本品中。 从用药的安全性出发,添加药物后的混合液应立即使用。如需存放,2~8℃下混合液的放置时间不宜超过24小时。
Fresenius Kabi AB
86978432000540;86978432000533;86978432000595;86978432000625;86978432000601;86978432000571;86978432000588;86978432000618
未进行该项实验且无可靠参考文献。
未进行该项实验且无可靠参考文献。
注射剂
1026ml[脂肪乳注射液(20%)200ml;复方氨基酸注射液(17)300ml;葡萄糖注射液(19%)526ml];2053ml [脂肪乳注射液(20%)400ml;复方氨基酸注射液(17)600ml;葡萄糖注射液(19%)1053ml];2566ml [脂肪乳注射液(20%)500ml;复方氨基酸注射液(17)750ml ;葡萄糖注射液(19%)1316ml];1540ml [脂肪乳注射液(
本品有四种包装规格。多聚复合膜塑料袋装,2566 ml/袋,2053 ml/袋,1540 ml/袋,1026 ml/袋。
密封,25℃以下,不得冰冻。包装应完整,如发生破损,不得使用。 使用前须将三腔内液体互相混合。当打开可撕裂封条、三腔内液体混合均匀后,在25℃下其物理与化学性质能稳定24小时。
253.00元
24个月
B05BA10
国药准字J20130180;国药准字J20130179;H20130854;H20130857;H20130855;H20130852;H20130853;H20130856
国家基本医疗保险和工伤保险药品

