星舒平/ MYQORZO说明书
Aficamten Tablets
阿夫凯泰
本品活性成份为阿夫凯泰。
化学名称:(R)-N-(5-(5-乙基-1,2,4-噁二唑-3-基)-2,3-二氢-1H-茚-1-基)-1-甲基-1H
吡唑-4-甲酰胺
化学结构式: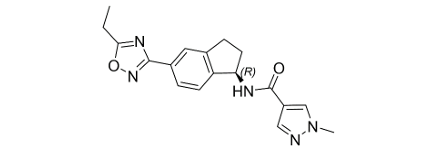
分子式: C18H19N5O2
分子量: 337.38
辅料:微晶纤维素,甘露醇,交联羧甲纤维素钠,羟丙纤维素,十二烷基硫酸钠,
硬脂酸镁,欧巴代QX紫色。
本品为紫色圆形薄膜包衣片,一面凹印“5”字样,另一面凹印“CK”字样。
本品用于治疗纽约心脏协会(NYHA)心功能分级II-III 级的梗阻性肥厚型心肌病(HCM)成人患者,以改善运动能力和症状。
本品使用前和使用期间的评价
不建议LVEF<55%的患者开始本品治疗或上调剂量。
患者在服用本品期间可能发生心力衰竭。滴定时需定期进行 LVEF 和Valsalva 动作后左心室流出道(Left Ventricular Outflow Tract,LVOT)压力阶差评估,以达到适当的Valsalva动作后LVOT压力阶差目标,同时保持LVEF≥50%。
推荐用法用量
本品的推荐起始剂量为5 mg,每日一次口服给药。每2周可进行一次剂量递增,每次增加5mg,直至达到维持剂量或最大推荐剂量20 mg。本品的维持剂量根据患者的LVEF 和LVOT压力阶差进行个体化滴定。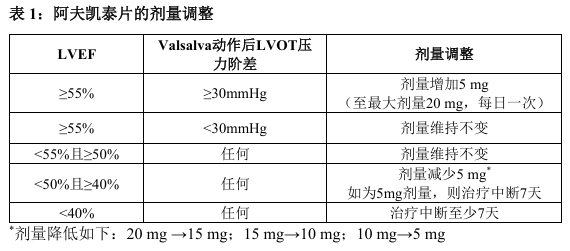
应在开始治疗、进行任何剂量调整或治疗中断后2周进行超声心动图评估。治疗中断后,当LVEF≥55%时,以5 mg的起始剂量重新开始治疗,并重新开始剂量滴定。
完成剂量调整确定维持剂量后,每3个月评估一次LVEF和Valsalva动作后LVOT压力阶差。对于出现并发疾病(例如,重度感染或COVID-19)、新发心律失常(例如,新发或未受控制的房颤或其他未受控制的快速性心律失常)或可能
损害收缩功能的任何其他疾病的患者,考虑监测LVEF并调整剂量(如需要)。在并发疾病或新发心律失常消退或稳定之前,请勿增加剂量。 应在每天大约相同的时间服用药物,每日一次,随餐或不随餐服用。按处方剂量服用一片片剂。随水整片吞服。
漏服或延迟给药
如果漏服一剂药物,应在同一天尽快服用。下一次计划给药应在第二天的常规时间进行。本品不应在同一天给药两次。
肾功能损害
轻度(肾小球滤过率估计值 [eGFR] 60-89 mL/min/1.73 m2)至中度(eGFR 30-59 mL/min/1.73 m2)肾损害患者无需调整标准推荐剂量和剂量滴定方案。由于尚未在重度肾损害(eGFR<30 mL/min/1.73 m2)患者中进行研究,因此该人群应慎用本品。
肝功能损害
轻度(Child-Pugh A 级)或中度(Child-Pugh B 级)肝损害患者无需调整标准推荐剂量和剂量滴定方案。由于尚未在重度肝损害(Child-Pugh C 级)患者中进行研究,因此该人群应慎用本品。
合并治疗
对于正在接受伏立康唑、氟伏沙明、强效 CYP2C9 抑制剂或中效至强效CYP2C9 或 CYP3A 诱导剂稳定治疗的患者,应以推荐起始剂量5 mg每日一次开始阿夫凯泰治疗。对于计划开始使用伏立康唑、氟伏沙明、强效CYP2C9抑制剂或停用中效至强效CYP2C9或CYP3A诱导剂的患者,应降低本品剂量(20 mg → 10 mg;15 mg → 5 mg;10 mg → 5 mg)。对于目前正在接受5mg剂量的患者,应维持5 mg剂量。应评估开始使用抑制剂或停用诱导剂后的LVEF和LVOT压力阶差,并根据调整计量表进行剂量滴定。
临床试验经验
由于临床试验是在各种不同的条件下进行的,因此在一种药物的临床试验中观察到的不良反应发生率不能直接与另一种药物的临床试验中的发生率进行比较,也不能反映在实践中观察到的发生率。
在一项随机、双盲、安慰剂对照III期研究(SEQUOIA-HCM)中评价了本品的安全性。在282例梗阻性HCM成人患者中,142例患者接受了每日剂量为5 mg、10 mg、15 mg 或 20 mg 的阿夫凯泰,140例患者接受了安慰剂治疗。接受本品治疗患者的中位治疗持续时间为24.1周(范围:3.9-29.4周 )。 总体而言,5.6%接受本品治疗的患者和 9.3%接受安慰剂治疗的患者发生了严重不良事件。
>5%的患者发生且在阿夫凯泰片组更常见(与安慰剂组相比)的不良反应为高血压(7.7% vs. 2.1%)和心悸(7.0% vs. 2.9%)。
阿夫凯泰片组中≥5%的受试者报告的不良事件(与安慰剂组相比)有头痛(7.7% vs. 7.1%)、上呼吸道感染(6.3% vs. 8.6%)、呼吸困难(5.6% vs. 5.7%)。合格的 oHCM患者能够参加一项正在进行的、开放性、长期安全性和耐受性研究(FORESTHCM)。截至中期数据截止日期,FOREST-HCM 研究中的安全性特征与SEQUOIA-HCM研究中观察到的安全性特征一致。
对收缩功能的影响
在SEQUOIA-HCM研究中,阿夫凯泰组患者的基线LVEF均 值( SD)为 74.8%(5.48),安慰剂组为74.8%(6.26)。与本品的作用机制一致,在24周治疗期间,阿夫凯泰组LVEF 较基线的LS均值(SE)变化为-6.77%(0.55),安慰剂组为2.02%(0.55)。治疗结束后 4 周,阿夫凯泰和安慰剂组之间的平均LVEF 相似。
在24 周治疗期间,阿夫凯泰组5例(3.5%)患者和安慰剂组1例(0.7%)患者出现可逆性LVEF低于<50%(中位数:47%;范围:34%-49%)。 LVEF 低于50%期间并未中断治疗,且表现与临床心力衰竭不相关。
在中位暴露时间为13.96个月的包含335例受试者的安全性分析中共有9例受试者(2.7%)出现基线后LVEF < 50%,受试者未出现心力衰竭,所有4例受试者均在剂量降低或洗脱期后LVEF自行恢复至≥ 50%。
中国人群中的长期安全性
一项开放标签扩展研究评价了阿夫凯泰的长期安全性,该研究入组了40名参加了SEQUOIA-HCM 的符合条件的中国oHCM 患者。在中期分析时,所有参与者均完成了48周的治疗。该研究中观察到的安全性特征与在SEQUOIA-HCM中观察到的安全性特征一致。
禁止与以下药物合并使用:
• 氟康唑给药超过3天
• 利福平
心力衰竭风险 接受心肌肌球蛋白抑制剂的患者可能发生收缩功能障碍导致的心力衰竭。 本品可降低左心室射血分数(LVEF)。本品治疗前和治疗期间需进行超声心动图评估,以监测收缩功能障碍。不建议LVEF<55%的患者开始本品治疗。用药期间,如果LVEF<50%且≥40%,则需降低本品剂量。如果LVEF<40%或患者因收缩功能障碍而出现心力衰竭症状或临床状态恶化,则需中断本品给药。
心力衰竭
本品可降低心肌收缩力,并可降低LVEF。接受心肌肌球蛋白抑制剂的患者可能发生收缩功能障碍导致的心力衰竭。
出现严重并发疾病(例如,严重感染)或心律失常(例如,新发或未受控制的房颤)的患者发生收缩功能障碍和心力衰竭的风险可能更高。无症状性LVEF降低、并发疾病和心律失常需考虑进行额外监测。
治疗前和治疗期间定期评估患者的临床状态和LVEF,并相应调整本品剂量。新发或恶化的心律失常、呼吸困难、胸痛、疲劳、腿部水肿或N末端B型利钠肽前体(NT-proBNP)升高可能是心力衰竭的体征和症状,应及时进行心脏功能评价。
不建议LVEF<55%的患者开始本品治疗。
导致心力衰竭或丧失有效性的细胞色素P450相互作用
本品通过CYP2C9、CYP2D6和CYP3A酶代谢。开始使用一些对本品多种P450 代谢酶消除途径具有抑制作用的药物(例如,氟康唑、伏立康唑、氟伏沙明)、强效 CYP2C9 抑制剂以及停用中效至强效 CYP3A 诱导剂和中效至强效CYP2C9 诱导剂可能导致阿夫凯泰血药浓度升高,并增加因收缩功能障碍导致心力衰竭的风险(参见【禁忌】、【注意事项】和【药物相互作用】)。相反,开始使用一些可诱导P450的药物(例如,利福平、中效至强效CYP3A或CYP2C9诱导剂)可能导致阿夫凯泰血药浓度降低并丧失有效性(参见【禁忌】和【药物相互作用】)。
告知患者发生药物相互作用的可能性。建议患者在开始本品治疗之前和治疗期间告知医务人员所有合并用药(参见【药物相互作用】)。
尚无关于阿夫凯泰用药过量的报告。
阿夫凯泰用药过量的治疗包括:终止阿夫凯泰治疗,维持血流动力学稳定的支持性医疗措施,如密切监测生命体征、LVEF、以及管理患者的临床状态。本品过量服用会危及生命,并导致难以治疗的心跳停止。
风险总结 尚无关于孕妇使用本品的数据,因此无法确定是否存在与药物相关的重大出生缺陷或流产风险。尚不清楚孕妇使用阿夫凯泰是否会对胎儿造成伤害,阿夫凯泰仅应在潜在获益大于对胎儿的潜在风险时用于孕妇(参见【药理毒理】)。 目标人群发生重大出生缺陷和流产的估计背景风险未知。 临床注意事项 疾病相关母体和胚胎-胎儿风险 妊娠合并梗阻性HCM与早产风险增加相关(参见【药理毒理】)。风险总结 尚不清楚本品是否会排泄至人乳汁中或其对母乳喂养婴儿的影响。尚未确定本品在儿童患者中的安全性和有效性。SEQUOIA-HCM 研究中有 57 例 65 岁及以上的患者(参见【临床试验】)。 在SEQUOIA-HCM 研究中接受本品治疗的患者总数中,45例患者年龄为65-74岁,12例患者年龄为75岁及以上。 未观察到65岁及以上患者和年轻成人患者之间本品的安全性或有效性存在总体差异。75岁以上的患者高血压、心悸、头晕的发生率高于年轻患者。
体外研究
CYP 酶:在临床相关浓度下,预期阿夫凯泰不会抑制 CYP1A2、CYP2B6、CYP2C8、CYP2C19、CYP2D6 或 CYP3A4。在临床相关浓度下,预期阿夫凯泰不会诱导CYP1A2、CYP2B6或CYP3A4。
药物转运蛋白:阿夫凯泰不是药物转运蛋白的敏感底物。在临床相关浓度下,预期阿夫凯泰不会抑制BCRP、OCT2、OCT3、OAT1、OAT3、OATP1B1、OATP1B3、MATE1或MATE2-K药物转运蛋白。
体内研究
CYP 酶的抑制剂和诱导剂
表2提供了预测的和观察到的与选定的CYP抑制剂和诱导剂联合给药对阿
夫凯泰血浆暴露量的影响。
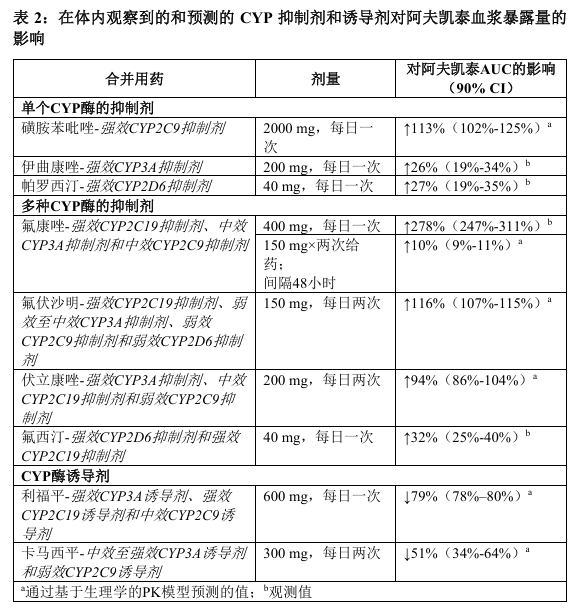
转运蛋白底物
P-gp 底物:单剂量20 mg 阿夫凯泰合并给药使达比加群(以达比加群酯形
式给药)的AUCinf增加26%(90% CI:12%-41%)。
其他药物影响阿夫凯泰血药浓度的可能性
阿夫凯泰主要由CYP2C9代谢,其次是CYP2D6和CYP3A,CYP2C19极少
参与其代谢。
已确定的和预测的与阿夫凯泰的潜在临床显著DDI
合并使用那些对参与阿夫凯泰消除的多种P450途径具有抑制作用的特定药
物、强效CYP2C9抑制剂、以及中效至强效CYP2C9或CYP3A诱导剂可能会影
响阿夫凯泰的暴露量(参见【注意事项】和【药理毒理】)。
表3提供了基于本品临床研究或使用基于生理学的药代动力学建模分析预测
的已确定或潜在的临床显著药物相互作用列表。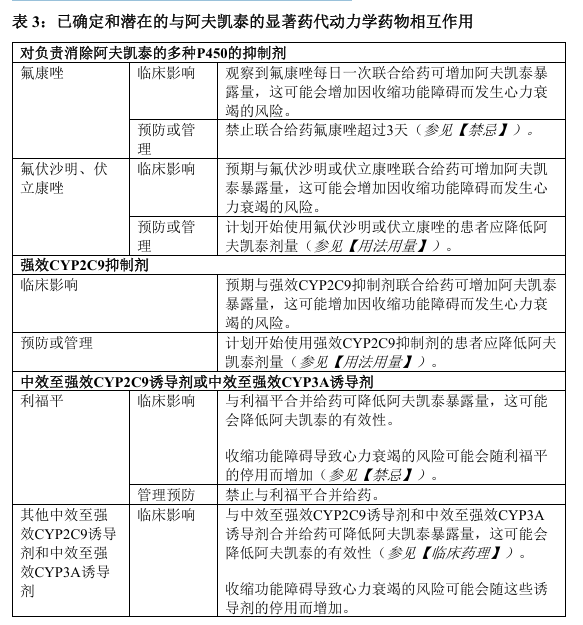

与阿夫凯泰无临床显著相互作用的药物
建立的生理PK模型预测DDI研究结果表明,与中效CYP2C9抑制剂、中
效或强效 CYP3A 抑制剂和中效或强效 CYP2D6 抑制剂联合给药对阿夫凯泰的
血浆暴露量无具有临床意义的影响。
阿夫凯泰影响其他药物血药浓度的潜力
预期阿夫凯泰与CYP酶或药物转运蛋白的敏感底物联合给药不会引起具有
临床意义的DDI(参见【药理毒理】)。
具有负性肌力作用的药物
β 受体阻滞剂、非二氢吡啶类钙通道阻滞剂、丙吡胺和胺碘酮用于治疗梗阻
性HCM,可能具有负性肌力作用。
在与这些药物联合给药的情况下,可安全开始并维持阿夫凯泰治疗;因此,
建议遵循常规剂量滴定指南(参见【用法用量】)。如果开始使用负性肌力药物合
并治疗,或者增加负性肌力药物的剂量,则应监测LVEF,直至达到稳定剂量并
显示出临床缓解。
群体PK建模表明,与β受体阻滞剂、钙通道阻滞剂、丙吡胺或胺碘酮联合
给药对阿夫凯泰的血浆暴露量无影响。
Patheon Inc.
86985485000014
阿夫凯泰是一种选择性、可逆性的心肌肌球蛋白变构抑制剂,可直接与心肌球蛋白的马达结构域结合,并阻止其进入产生力的状态。阿夫凯泰可缓解梗阻性肥厚型心肌病患者的左心室流出道梗阻。
遗传毒性
阿夫凯泰Ames 试验、大鼠肝细胞彗星试验和骨髓微核试验结果均为阴性。
生殖毒性
在大鼠生育力和早期胚胎发育毒性试验中,雌性和雄性大鼠经口给予阿夫凯泰达6 mg/kg/天和3 mg/kg/天,对交配、生育力、发情周期、雄性生殖评估或早期胚胎存活率未见明显影响。
妊娠大鼠于器官发生期经口给予阿夫凯泰2、6、9mg/kg/天,9 mg/kg/天组可见总吸收胎数、早期吸收胎数、着床后胚胎丢失率增加;对胚胎-胎仔发育的未见不良反应剂量水平(NOAEL)为6 mg/kg/天,以暴露量(AUC0-24h)计,约为人最大推荐剂量(MRHD,20 mg)的 3.5倍。妊娠兔于器官发生期经口给予阿夫凯泰5、10、20/15mg/kg/天,20/15mg/kg 组可见部分动物死亡,≥5mg/kg组动物体重增长缓慢及摄食量降低,未见对胚胎-胎仔发育的影响。对母体毒性的NOAEL为10mg/kg/天,对胚胎-胎仔发育毒性的NOAEL为15mg/kg/天 ,以 AUC0-24h计,约为MRHD的0.05倍和0.17倍。
在围产期毒性试验中,大鼠从妊娠第6天至哺乳期第21天,经口给予阿夫凯泰0.5、1.5和6.0 mg/kg/天,6.0 mg/kg 剂量下可见母体体重减轻、心脏重量增加和幼仔存活率降低,0.5和1.5mg/kg/天剂量下未见母体及子代异常。
致癌性
Tg.rasH2 小鼠连续 6 个月经口给予阿夫凯泰 0.5、1.0 和 2.0 mg/kg/天(以AUC0-24h计,高剂量约为MRHD的2倍),所有受试动物均未见致癌性。
大鼠2年致癌性试验中,经口给予阿夫凯泰 0.5、1、2(雄性动物)/3(雌性动物)mg/kg/天,高剂量组雌雄动物因存活率降低分别于91周、68周停止给药,并于96周、79和80周处以安乐死,溶媒组动物于100至103周安乐死,给药组动物均未见致癌性。以AUC0-24h计,大鼠3 mg/kg/天约为MRHD的3倍。
其他
阿夫凯泰进行了大鼠最长6个月和犬最长9个月的重复给药毒性试验,剂量范围 0.25~9.0 mg/kg/天,高剂量(在大鼠中剂量≥6 mg/kg/天,在犬中剂量≥2 mg/kg/天)下可见心脏重量增加、心房/心室扩张、扩张型心肌病、死亡,与阿夫凯泰抑制心肌肌球蛋白的药理作用相关。大鼠6个月重复给药毒性试验NOAEL为1.5mg/kg/天,犬 9 个月重复给药毒性试验 NOAEL 为 1.0 mg/kg/天,以 Cmax计,约为MRHD的2.9倍和7.3倍;以AUC0-24h计,约为 MRHD的1.7倍和3.0倍。
在每日一次、多次给予1 mg至75 mg剂量的阿夫凯泰后,阿夫凯泰的暴露
量与剂量成比例增加。健康受试者和oHCM患者的阿夫凯泰 PK相似。各剂量
水平的阿夫凯泰蓄积比的几何平均值相似,范围为4.57-4.82。
吸收
阿夫凯泰可被迅速吸收,中位浓度达峰时间(Tmax)为 1.50-2.00小时。尚不
清楚口服给药后阿夫凯泰的生物利用度。
食物的影响
随高脂、高热量餐给药后,未观察到阿夫凯泰AUC和Cmax出现具有临床意
义的差异。
分布
阿夫凯泰与血浆蛋白的结合率约为90%,分布容积为309 L。阿夫凯泰的全
血-血浆分配比为0.94。
消除
在 oHCM 患者中,阿夫凯泰的中位终末半衰期(t½)和至稳态时间分别为
约80小时和17天。预期大多数(约95%)oHCM患者的t½小于155小时,并
在进行阿夫凯泰每日给药后第33天达到稳态。稳态时,每日一次给药的血药浓
度峰谷比约为1.2。总清除率为2.6 L/h,肾脏清除率<总清除率的0.1%。
阿夫凯泰在人体内广泛代谢,主要代谢途径包括 CYP2C9(50%)、 CYP3A
(26%)和 CYP2D6(21%), CYP2C19(3%)极少参与其代谢。阿夫凯泰主要
代谢为两种无药理学活性的代谢物,即CK-3834282 和 CK-3834283,在循环系
统中的浓度水平分别约为血浆中母体化合物的56%和103%。
单次给予20 mg放射性标记剂量的阿夫凯泰后,32%(0.55%为原型阿夫凯
泰)经尿液排泄,58%(5.0%为原型阿夫凯泰)经粪便排泄。
特殊人群
基于群体药代动力学分析,未观察到年龄(18-83岁)、性别或人种在阿夫凯
泰的药代动力学出现具有临床意义的差异。
肾功能损害
群体药代动力学分析表明,在轻度至中度肾功能损害(eGFR:≥30
mL/min/1.73 m²)患者中,阿夫凯泰的药代动力学并无临床意义的差异。重度肾功能损害的影响尚不清楚。
肝功能损害
根据I期临床研究,在轻度至中度肝功能损害患者中,阿夫凯泰的药代动力
学并无临床意义的差异。重度肝功能损害的影响尚不清楚。
片剂
5 mg
密封,不超过25℃保存。请将本品放在儿童不能接触的地方。
24个月
国药准字HJ20250147

