信立安说明书
Linaprazan Glurate Capsules
戊二酸利那拉生酯
本品活性成份为戊二酸利那拉生酯。
化学名称:5-(2-(8-((2,6-二甲基苄基)氨基)-2,3-二甲基咪唑并[1,2-a]吡啶-6-甲酰
胺基)乙氧基)-5-氧代戊酸。
分子式:C26H32N4O5
分子量:480.56
辅料:乳糖、微晶纤维素、交联羧甲纤维素钠、十二烷基硫酸钠、硬脂富马酸
钠、胶态二氧化硅、明胶空心胶囊。
本品为乳白色胶囊,内容物为白色至类白色粉末。
反流性食管炎
口服,空腹服用。成人每日1次,每次50mg,连续治疗8周。
已在1项随机、双盲、阳性对照III期临床试验中评价了戊二酸利那拉生酯胶囊的安全性,共有283例成人反流性食管炎患者接受了戊二酸利那拉生酯胶囊50mg每日一次治疗。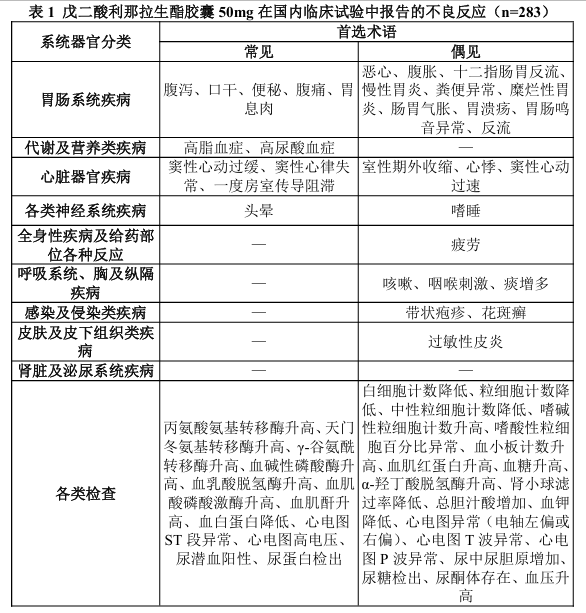
本品I期临床试验健康受试者报告了与药物相关的心电图QT间期延长,严重程度均为1级,未进行干预于当日或隔日恢复正常,在反流性食管炎II期和III期临床试验中未发现与QT间期延长相关的不良反应。
1.对本品中任何成份过敏的患者禁用。
2.正在服用阿扎那韦、奈非那韦或者利匹韦林的患者禁用。
1. 服用本品有可能掩盖胃恶性肿瘤的症状,开始使用本品前应先排除恶性肿瘤的可能。
2. 临床试验中已经报告了肝功能异常,其中许多发生在治疗开始后不久。应进行密切观察,如有肝功能异常证据或出现提示肝功能不全的体征或症状,应采取包括停药在内的适当措施。尚无肝功能损伤患者使用戊二酸利那拉生酯的经验,此类患者应慎用。
3. 戊二酸利那拉生酯会导致胃内pH升高,因此不建议本品与吸收依赖于胃内pH 的药物同服。
4. 应用质子泵抑制剂使胃酸水平下降时,可能导致胃肠道细菌数量增加,可能增加沙门氏菌、弯曲杆菌、艰难梭菌等细菌的感染风险。多项国外开展的观察性研究(主要涉及住院患者)报告在接受质子泵抑制剂治疗的患者中,艰难梭菌所引起的胃肠道感染风险增加。伪膜性结肠炎可能是根除幽门螺杆菌时合并使用了抗生素。如果出现腹痛或频繁腹泻,应采取包括停药在内的适当措施。
5. 国外开展的几项观察性研究报道,质子泵抑制剂治疗期间骨质疏松相关性髋关节、腕关节或脊柱骨折的风险增加。接受高剂量或长期(≥1年)治疗的患者骨折风险增加更为明显。
6. 长期(如3年以上)服用胃酸抑制剂导致胃酸减少或缺乏,可能引起维生素B12 吸收障碍。已有文献报告,长期服用胃酸抑制剂与维生素B12缺乏有关。
7. 在接受至少3个月以及绝大多数在接受一年质子泵抑制剂治疗的患者中,极少有无症状和伴有症状的低镁血症病例报道。上述严重不良反应包括手足抽搐,心律不齐和癫痫发作。低镁血症可能导致低钙血症和/或低钾血症,并可能加重高危患者的潜在低钙血症。对于绝大多数患者,纠正低镁血症,需补镁治疗及停用质子泵抑制剂。预期需延长质子泵抑制剂治疗或合并用药如地高辛或能导致低镁血症(如,利尿剂)的药物,医学专业人士可考虑在开始质子泵抑制剂治疗前及定期监测血镁浓度。对有低钙血症风险的患者(如甲状旁腺功能减退症),考虑在开始使用本品前及治疗时定期监测血镁和血钙的浓度。如果低钙血症治疗无效,考虑停止使用质子泵抑制剂。
8. 胃酸抑制剂可引起高胃泌素血症。持续、显著的胃泌素血症可能导致肠嗜铬细胞生长,促进类癌和神经内分泌肿瘤的发生。戊二酸利那拉生酯临床试验中观察到胃泌素升高,长期影响尚不确定。
9. 已有研究报道,长期给予钾离子竞争性酸阻滞剂观察到良性胃息肉。质子泵抑制剂长期使用会导致胃底息肉的风险增加,尤其是长期使用一年以上。大多数发展为胃底息肉的质子泵抑制剂使用者是无症状的,只是在内窥镜检查中偶然发现了有胃底息肉。
10. 尚无本品超过8周的长期服用临床数据。尚未研究本品用于反复发作的反流性食管炎患者的维持治疗。
11. 尚无肾功能损伤患者使用本品的经验,此类患者应慎用。
尚无药物过量的研究及过量使用的报道。临床试验中,健康受试者单次口服本品225mg后可耐受,反流性食管炎患者连续4周每日口服100mg后可耐受。如果发生用药过量,应监测患者有关毒性的症状,必要时给予对症治疗。
尚无孕妇使用本品的临床数据。非临床研究数据见。戊二酸利那拉生酯可通过胎盘屏障,妊娠期禁用本品。迄今尚未有评价本品在哺乳期受试者中的临床研究。尚不清楚本品是否排泄到人乳汁中。在一项大鼠毒理学研究中,已经证明本品可排泄到乳汁中。建议在哺乳期避免服用本品,必须给药时,应首先停止哺乳。尚无本品用于18岁以下儿童或青少年的临床数据。通常老年人的肝功能或者肾功能等生理功能低下,老年患者应慎用。
本品会导致胃内pH升高,提示对于胃内pH是口服生物利用度重要决定因素的药物,本品可能影响其吸收。故不应与阿扎那韦、利匹韦林同服,应谨慎与奈非那韦、伊曲康唑、酪氨酸激酶抑制剂(吉非替尼、尼洛替尼、厄洛替尼)同服,因为此类药物的作用可能减弱。本品应谨慎与地高辛、甲基地高辛同服,因为此类药物的作用可能会增强。
本品主要通过肝脏药物代谢酶CYP3A4进行代谢。目前尚未开展本品与CYP3A4抑制剂或诱导剂的相互作用研究。因此应谨慎与CYP3A4抑制剂或诱导剂同时服用。
86984595000013
戊二酸利那拉生酯及其活性代谢产物Linaprazan通过抑制H+、K+-ATP酶活性而抑制胃酸分泌,从而抑制胃肠道上部黏膜损伤的形成。戊二酸利那拉生酯抑制H+、K+-ATP 酶活性的IC50为436.2nM,Linaprazan 抑制 H+、K+-ATP 酶活性的IC50为40.21nM。
遗传毒性
戊二酸利那拉生酯Ames试验、中国仓鼠肺成纤维细胞染色体畸变试验、大鼠体内微核试验结果均为阴性。
生殖毒性
在大鼠生育力与早期胚胎发育试验中,经口给予戊二酸利那拉生酯6、30、150mg/kg/天,雄鼠自交配前4周开始给药至交配成功,雌鼠自交配前2周开始给药至妊娠第6日(GD6)。各剂量组未见对雌雄大鼠生育力与早期胚胎发育的明显影响,NOAEL为150mg/kg/天。以暴露量计,高剂量组的戊二酸利那拉生酯约为临床推荐剂量50mg/天的6.7倍。各剂量组活性代谢产物Linaprazan暴露量与给药剂量的线性关系不明显,末次给药最大暴露量约为临床推荐剂量50mg/天暴露量的2.4倍(雌鼠)、1.3倍(雄鼠)。
在大鼠胚胎-胎仔发育试验中,妊娠大鼠于器官发生期(GD6~GD15)经口给予戊二酸利那拉生酯6、30、150mg/kg/天,各剂量组未见与给药相关的母体毒性及对胚胎-胎仔发育的明显影响,NOAEL为150mg/kg/天。以暴露量计,高剂量组的戊二酸利那拉生酯约为临床推荐剂量50mg/天的3.0倍。各剂量组活性代谢产物Linaprazan 暴露量与给药剂量的线性关系不明显,末次给药最大暴露量约为临床推荐剂量50mg/天暴露量的1.7倍。
在兔胚胎-胎仔发育试验中,妊娠兔于器官发生期(GD6~GD19)经口给予戊二酸利那拉生酯3、10、20mg/kg/天。高剂量组(以暴露量计,戊二酸利那拉生酯、linaprazan分别约为临床推荐剂量50mg/天的6.9倍、1.4倍)可见流产和早产,食量降低,粪便异常,体重降低,子宫连胎重降低,吸收胎率、平均晚期吸收胎数、晚期吸收胎率、着床后丢失率升高,平均活胎数、活胎率降低,胎仔体重降低。低、中剂量组(以暴露量计,戊二酸利那拉生酯分别约为临床推荐剂量50mg/天的0.4倍、4.4倍,linaprazan分别约为临床推荐剂量50mg/天的0.2倍、1.2倍)可见胎仔输尿管蛇形发生例数增加,高剂量组未见增加。胎仔血浆中可检测到linaprazan暴露,并呈剂量相关性。
在大鼠围产期毒性试验中,自GD6至哺乳期21日(LD21)经口给予戊二酸利那拉生酯6、30、150mg/kg/天。中剂量组可见1只妊娠母鼠死亡及宫内吸收胎/死胎。各剂量组可见F1代双耳、全身苍白,离乳前体重降低,离乳后初期体重及食量降
低;中、高剂量组还可见F1代被毛粗糙;高剂量组还可见F1代睁眼达标时间延长。
各剂量组F0代戊二酸利那拉生酯、linaprazan暴露量相近。F0代NOAEL为6mg/kg/天(以暴露量计,戊二酸利那拉生酯、linaprazan分别约为临床推荐剂量50mg/天的0.9 倍、1.3 倍),未获得F1代的NOAEL剂量,F2代NOAEL为150mg/kg/天(以暴露量计,戊二酸利那拉生酯约为临床推荐剂量50mg/天的3.5倍;各剂量组末次给药linaprazan 最大暴露量约为临床推荐剂量50mg/天暴露量的2.4倍)。伴随毒代研究显示,戊二酸利那拉生酯、linaprazan可通过胎盘屏障,可经乳汁分泌。
致癌性
在Tg.rasH2 小鼠26周致癌性试验中,经口给予戊二酸利那拉生酯30、100和300mg/kg/天(以暴露量计,戊二酸利那拉生酯分别约为临床推荐剂量50mg/天暴露量的0.25、1.2、0.4 倍(雄鼠)/0.6、1.1、1.2 倍(雌鼠);Linaprazan 分别约为临床推荐剂量50mg/天暴露量的2.3、3.6、4倍(雄鼠)/1.8、5.5、4倍(雌鼠),各剂量组可见腺胃黏膜增生、粘液细胞和/或上皮细胞增生、黏膜/固有层/黏膜下层炎细胞浸润、黏膜/肌层空泡形成、腺胃黏膜隐窝扩张和隐窝嗜酸性物质,高剂量组雄
鼠可见腺胃上皮细胞非典型性增生,各剂量组肿瘤发生率未见明显升高。在大鼠两年致癌性试验中,经口给予戊二酸利那拉生酯6、30和150mg/kg/天(以暴露量计,戊二酸利那拉生酯分别约为临床推荐剂量50mg/天暴露量的0.9、4.7、10.0 倍(雄鼠)/1.0、6.2、8.0 倍(雌鼠);Linaprazan分别约为临床推荐剂量50mg/天暴露量的0.77、1.8、2.6倍(雄鼠)/1.8、4.6、6.8倍(雌鼠)),各剂量组可见胰腺腺泡细胞腺瘤发生率升高,各剂量组雌鼠和6mg/kg/天剂量组雄鼠腺胃神经内分泌细胞瘤发生率升高。6mg/kg/天剂量组雄鼠可见心脏施万细胞瘤、肾脏腺癌、甲状旁腺腺瘤、甲状腺滤泡细胞腺瘤,30mg/kg/天剂量组雄鼠可见肝细胞癌、胰腺细胞癌,30mg/kg/天剂量组雌鼠可见卵巢粒层细胞瘤,150mg/kg/天剂量组雄鼠可见皮肤施万细胞瘤、睾丸间质细胞瘤、肾上腺腺瘤。
胶囊剂
50mg
聚酰胺/铝/聚氯乙烯冷冲压成型固体药用复合硬片、药用铝箔包装。7粒/板,1 板/盒;7粒/板,2板/盒。
避光,不超过30℃密闭保存。
24个月
国药准字H20240042

