圣赫途说明书
Zongertinib Tablets
宗艾替尼
本品活性成份为:宗艾替尼。
化学名称:N-{1-[8-({3-甲基-4-[(1-甲基-1 H-1,3-苯并二唑-5-基)氧基]苯基}氨基)-[1,3]二氨杂[5,4-d]嘧啶-2-基]哌啶-4-基}丙-2-烯酰胺
分子式:C29H29N9O2
分子量:535.60
辅料:醋酸羟丙甲纤维素琥珀酸酯,微晶纤维素,甘露醇,交联羧甲纤维素钠,胶态二氧化硅,硬脂富马酸钠,薄膜包衣预混剂(胃溶型)。
本品单药适用于治疗存在 HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。该适应症是基于单臂临床试验的结果给予的附条件批准。该适应症的完全批准将取决于开展的确证性试验的临床获益。
患者选择
接受本品治疗的患者应采用经充分验证的检测方法检测到 HER2(ERBB2)激活突变。HER2 检测必须在专业实验室进行,以确保结果的可靠性。
推荐剂量
本品的推荐剂量为 120 mg(2 片),口服,每日 1 次。治疗应持续直至患者出现疾病进展或出现不可接受的毒性。可与或不与食物同服。应用水整片送服。请勿掰开、压碎或咀嚼片剂。如患者漏服本品一次,且距离下次服药时间超过 12 小时,应补服本品。如不足 12 小时,则跳过此漏服的剂量,并在次日的计划时间按照计划的剂量继续服药。
针对不良反应进行的剂量调整
针对不良反应推荐的剂量调整请参见表 1。在第一次将剂量降低至 60 mg 每日一次后,如仍无法耐受本品的患者必须永久停止治疗。
表 1. 本品的推荐剂量调整(针对不良反应)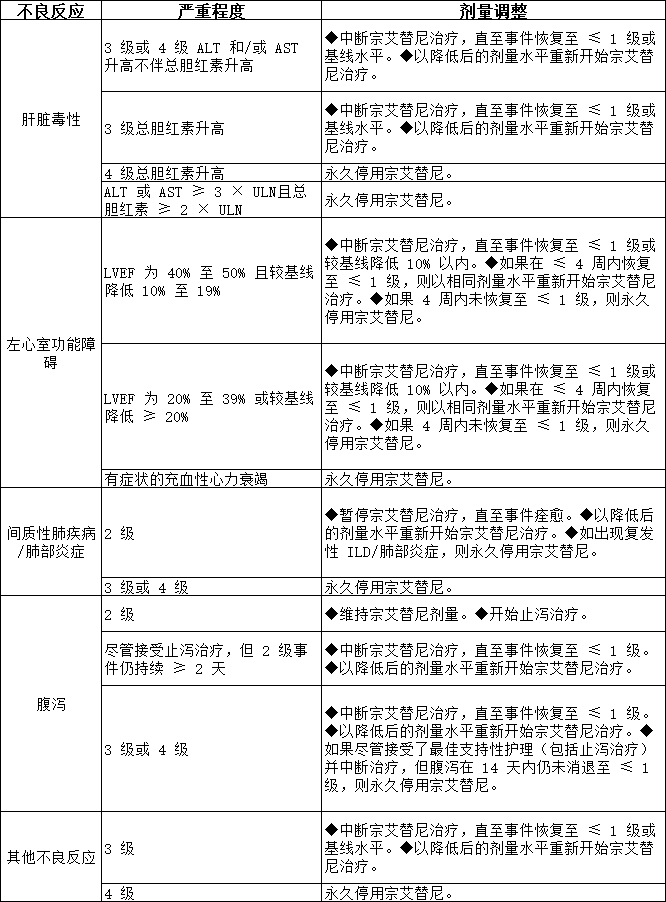
特殊人群
肾功能损害患者
轻度肾功能损害患者无需调整剂量。尚未研究本品在中度肾功能损害、重度肾功能损害或终末期肾脏疾病患者中的安全性、有效性和药代动力学。
肝功能损害患者
轻度肝功能损害患者无需调整剂量。尚未确定宗艾替尼在既往存在中度或重度肝功能损害患者中的安全性和有效性。不建议既往存在中度或重度肝功能损害患者接受本品的治疗。
安全性特征总结
汇总安全性人群反映了在 Beamion LUNG-1 中 260 例携带 HER2(ERBB2)(包括酪氨酸激酶结构域及酪氨酸激酶结构域外)突变的不可切除或转移性非鳞状 NSCLC 患者接受宗艾替尼单药 20 mg 每日一次口服给药的暴露量。在 260 例接受宗艾替尼治疗的患者中,58% 的患者暴露时间 ≥ 6 个月,13% 的患者暴露时间>1 年。在该汇总安全性人群中,最常见(>20%)的不良反应为腹泻(53%)、肝脏毒性(27%)、皮疹(27%)、疲劳(22%)和恶心(21%)。最常见( ≥ 2%)的 3 级或 4 级实验室检查异常为淋巴细胞减少(9%)、丙氨酸氨基转移酶升高(5%)、天门冬氨酸氨基转移酶升高(4.3%)、钾减少(2.7%)和γ-谷氨酰转移酶升高(2.7%)。接受宗艾替尼治疗的 HER2 酪氨酸激酶结构域外突变与 HER2 酪氨酸激酶域突变的 NSCLC 患者的总体安全性特征基本一致。
Beamion LUNG-1
Beamion LUNG-1 在 105 例携带 HER2 酪氨酸激酶结构域(TKD)突变且既往接受过治疗的不可切除或转移性非鳞状 NSCLC 患者中评价了宗艾替尼的安全性。所有患者既往均接受过含铂化疗,其中 34 例患者既往接受过靶向 HER2 的抗体偶联药物(ADC)治疗。患者接受宗艾替尼单药 120 mg 每日一次治疗,直至疾病进展或出现不可接受的毒性。在接受宗艾替尼治疗的患者中,72% 的患者暴露时间 ≥ 6 个月,30% 的患者暴露时间>1 年。接受宗艾替尼治疗的患者的中位年龄为 61 岁(范围 30-85 岁),69% 为女性,40% 为白人,49% 为亚洲人,0% 为黑人或非裔美国人;11% 的人种数据未知;1.9% 为西班牙裔或拉丁裔;33% 的患者美国东部肿瘤协作组(ECOG)体能状态评分为 0 分,67% 的患者 ECOG 体能状态评分为 1 分。
接受宗艾替尼治疗的患者中有 34% 的患者发生了严重不良反应。有 ≥ 2% 的患者发生的严重不良反应包括呼吸困难(4.8%)、肺栓塞(4.8%)、肝脏毒性(2.9%)和感染性肺炎(2.9%)。接受宗艾替尼治疗的患者中,有 1% 的患者因感染性肺炎发生致死性不良反应。2.9% 的患者因不良反应而永久停用宗艾替尼。导致永久停用宗艾替尼的不良反应为肝脏毒性、血碱性磷酸酶升高,呼吸困难、γ-谷氨酰转移酶升高,咯血和发热。28% 的患者因不良反应而中断宗艾替尼治疗。有 ≥ 2% 的患者发生的需要中断给药的不良反应为肝脏毒性、射血分数降低和皮疹。
7% 的患者因不良反应而降低宗艾替尼剂量。 ≥ 1% 的患者发生的需要降低剂量的不良反应为肝脏毒性,射血分数降低,血肌酸激酶升高,γ-谷氨酰转移酶升高和中性粒细胞计数降低。
接受宗艾替尼治疗的患者中,有 < 15% 的患者发生的临床相应包括口腔黏膜炎、皮肤干燥、瘙痒和外周神经病变。
无明确禁忌,但需警惕严重不良反应风险。
肝脏毒性
宗艾替尼可引起重度和危及生命的肝脏毒性,包括药物诱导的肝损伤。在汇总安全性人群中,根据不良反应数据,接受宗艾替尼治疗的患者中有 27% 的患者出现肝脏毒性。接受宗艾替尼治疗的患者中有 1.5% 的患者发生 3 级药物诱导的肝损伤,0.4% 的患者发生 4 级药物诱导的肝损伤。接受宗艾替尼治疗的患者中有 0.4% 的患者发生 3 级肝衰竭。根据实验室数据,接受宗艾替尼治疗的患者中有 35% 的患者发生丙氨酸氨基转移酶(ALT)升高,其中 4.3% 为 3 级事件,1.2% 为 4 级事件。
接受宗艾替尼治疗的患者中有 31% 的患者发生天门冬氨酸氨基转移酶(AST)升高,其中 3.5% 为 3 级事件,0.8% 为 4 级事件。接受宗艾替尼治疗的患者中有 20% 的患者发生胆红素增加,其中 0.8% 为 3 级事件,0.4% 为 4 级事件。8% 的患者因肝脏毒性不良反应而暂停宗艾替尼治疗,3.5% 的患者降低剂量,1.5% 的患者永久停药。
开始宗艾替尼给药前,在基线时应监测肝功能检查,包括 ALT、AST 和总胆红素,前 12 周内每 2 周监测一次,然后根据临床指征每月监测一次,对出现转氨酶升高的患者需进行更频繁的检查。建议根据不良反应的严重程度,考虑中断给药、降低剂量或永久停用宗艾替尼。
左心室功能障碍
宗艾替尼可导致重度左心室功能障碍。使用抗 HER2 治疗(包括宗艾替尼)时可能发生左心室射血分数(LVEF)降低。尚未在存在具有临床意义的心脏病史或治疗开始前 LVEF 低于 50% 的患者中对宗艾替尼治疗进行研究。在汇总安全性人群中,接受宗艾替尼治疗的患者中有 6% 的患者报告了 LVEF 降低,其中有 1.9% 的患者为 3 级。2 例发生 3 级 LVEF 降低的患者需要永久停用宗艾替尼。至发生 LVEF 降低的中位时间为 9 周(范围:2.9-63 周)。开始宗艾替尼治疗前,应评估 LVEF,并在治疗期间定期和在有临床指征时进行监测。建议根据不良反应的严重程度,考虑中断给药、降低剂量或永久停用宗艾替尼。
间质性肺疾病/肺部炎症
宗艾替尼可引起重度和危及生命的间质性肺疾病(ILD)/肺部炎症。在汇总安全性人群中,接受宗艾替尼治疗的患者中有 1.2% 的患者(N = 3)发生 ILD/肺部炎症。至首次发生 ILD/肺部炎症的中位时间为 19 周(范围:6-65 周)。1 例患者在肺部炎症痊愈后恢复治疗;1 例患者需要永久停药;1 例患者在宗艾替尼停药后(>30 天),死于未好转的肺部炎症。应监测患者是否出现提示 ILD/肺部炎症的新发或恶化症状(例如呼吸困难、咳嗽、发热)。建议根据确诊 ILD/肺部炎症的严重程度,考虑中断给药、降低剂量或永久停用宗艾替尼。
胚胎-胎儿毒性
基于动物研究结果和作用机制,对妊娠女性给予宗艾替尼时可能会造成胎儿伤害。在一项动物生殖研究中,妊娠大鼠在器官于形成期间接受宗艾替尼经口给药,在母体暴露量 ≥ 人体暴露量(基于推荐剂量下的 AUC)的 19 倍时,可导致其结构异常和生长改变。应向妊娠女性和有生育能力的女性告知本品对胎儿的潜在风险。建议有生育能力的女性在宗艾替尼治疗期间和末次给药后 2 周内采取有效的避孕措施。
尚不确定本品在 18 岁以下儿童和青少年的患者中的安全性和有效性。
Hovione Farmaciencia S.A.
86980023000457
宗艾替尼是一种人表皮生长因子受体-2(HER2)选择性酪氨酸激酶抑制剂,对人表皮生长因子受体 1(人 EGFR/HER1)无影响。宗艾替尼能够不可逆地抑制 HER2 激酶活性,阻断 HER2 激活的下游信号传导。体外细胞增殖试验中,宗艾替尼可抑制 HER2 野生型以及 HER2 突变(包括 HER2 外显子 20 插入突变)驱动的肿瘤细胞的生长。在体内,宗艾替尼在 HER2 突变的人肿瘤细胞小鼠异种移植瘤模型中可见肿瘤生长抑制作用。
重复给药毒性
在最长至 13 周的经口重复给药毒性研究中,宗艾替尼在 20 mg/kg 剂量下(暴露量约为人体暴露量的 0.7 倍[基于推荐剂量 120 mg/天下的 AUC])可诱导犬口腔粘膜出现不良反应。在一项大鼠 4 周毒性研究中,在 270 mg/kg 剂量(以未结合 AUC 计,约为人推荐剂量下暴露量的 6.3 倍)下观察到肾上腺病变(肥大、空泡形成增加和束状带/网状带单细胞坏死)。所有这些影响均可逆。
遗传毒性
宗艾替尼的 Ames 试验、大鼠体内彗星试验和大鼠体内外周血微核试验结果均为阴性。
生殖毒性
未对宗艾替尼开展生育力和早期胚胎发育试验。大鼠连续 13 周重复给药毒性试验中,宗艾替尼在 90 mg/kg/天剂量下(以未结合 AUC 计,约为人推荐剂量下暴露量的 3 倍)可引起雌性大鼠子宫萎缩以及宫颈和阴道增生/角化过度,在恢复期末未观察到这些变化。
大鼠胚胎-胎仔发育毒性剂量探索试验中,雌性妊娠大鼠于器官发生期每天 1 次经口给予宗艾替尼,在 ≥ 90 mg/kg 天剂量下(以未结合 AUC 计,约为人推荐剂量下暴露量的 5.2 倍)可见胚胎-胎仔死亡(在最高剂量 270 mg/kg 下无活体着床)。大鼠胚胎-胎仔发育毒性正式试验中,雌性妊娠大鼠于器官发生期每天 1 次经口给予宗艾替尼 10、30、60 mg/kg,在 ≥ 30 mg/kg 天剂量下(以未结合 AUC 计,约为人推荐剂量下暴露量的 3 倍)可见(尾椎和颈椎、趾骨、跟骨、下颌骨)骨化延迟增加,在 60 mg/kg/天剂量下(以未结合 AUC 计,约为人推荐剂量下暴露量的 3.3 倍)可见肾脏(肾盂扩张)和输尿管(扩张和/或弓形)变异增加。
兔胚胎-胎仔发育毒性剂量探索试验中,雌性妊娠兔于器官发生期每天 1 次经口给予宗艾替尼,在 150 mg/kg/天剂量下(以总 AUC 计,约为人推荐剂量下暴露量的 2.3 倍)可见母体毒性以及流产。兔胚胎-胎仔发育毒性正式试验中,在 80 和 120 mg/kg/天(以总 AUC 计,约为人推荐剂量下暴露量的 0.7 倍和 1.3 倍)剂量下可见胎仔胸骨骨化延迟的发生率轻度增加。
致癌性
宗艾替尼未开展致癌性试验。
本品基于替代终点获得附条件批准上市,暂未获得长期临床终点数据,尚待上市后进一步确证。Beamion LUNG-1 是一项单臂、开放性、多中心、多队列试验,队列 1 入组了至少接受一种系统性治疗,且携带 HER2(ERBB2)酪氨酸激酶域激活突变的不可切除或转移性非鳞状 NSCLC 患者(包含稳定的脑转移患者)。该队列排除了存在活动性脑转移或 ECOG 体能状态>1 分的患者。根据患者提供的组织当地检测结果判定是否存在 HER2(ERBB2)突变,前瞻性选择接受宗艾替尼片治疗的患者。使用 Oncomine Dx Target Test(Life Technologies Corporation,Tissue-test)对 Beamion LUNG-1 的样本进行回顾性检测。
主要有效性结局指标为盲态独立中心审查委员会(BICR)根据实体瘤疗效评价标准(RECIST)第 1.1 版评估的客观缓解率(ORR)。其他次要结局指标为 BICR 根据 RECIST1.1 评估的缓解持续时间(DOR)。共有 75 例患者持续接受本品推荐剂量 120 mg 每日一次治疗,直至出现疾病进展或出现不可接受的毒性。研究人群的特征包括:女性(68.0%)、亚洲人(53.3%)、白人(32.0%)。基线 ECOG 体能状态评分为 0 分(37.3%)或 1 分(62.7%)。
65.3% 的患者为从不吸烟者;100% 的患者存在 ERBB2 酪氨酸激酶结构域突变。患者的中位年龄为 62 岁(范围:30-80)。所有患者在筛选时均存在转移灶:37.3% 的患者存在稳定的脑转移灶。既往治疗方案的中位数为 1(范围:1-10):100% 的患者接受过铂类药物治疗,76.0% 的患者接受过 PD-1/PD-L1/CTLA-4 阻断性抗体治疗。6 例患者接受过靶向 HER2 的抗体偶联药物(ADC)治疗,无患者接受过 HER2 酪氨酸激酶抑制剂(TKI)治疗。
在队列 1 的 75 例患者中,28 例患者在基线时存在稳定的脑转移灶(可测量和不可测量病灶),为符合神经肿瘤学脑转移缓解评估(RANO-BM)标准的可评价患者。在这 28 例患者中,11 例(39.3%,95%CI23.6%,57.6%)患者观察到颅内病灶缓解,包括 4 例 CNS 完全缓解患者(14.3%):72.7% 的缓解者观察到颅内病灶缓解持续时间 ≥ 6 个月。在 20 例缓解可评价的携带酪氨酸激酶结构域外 HER2(ERBB2)突变的非鳞状 NSCLC 患者队列(队列 3)中评价了宗艾替尼。6 例患者达到部分缓解;3 例携带 S310F 突变(DOR(月):2.8,7.1 + ,9.7 + )的患者和 3 例携带 V659E 突变(DOR(月):4.2,7.0 + ,8.4 + )的患者( + 表示正在缓解)。
在 31 例既往接受过含铂化疗和靶向 HER2 的抗体偶联药物(ADC)治疗的 HER2(ERBB2)激酶结构域突变阳性非鳞状 NSCLC 患者队列(队列 5)中评价了宗艾替尼。在这些患者中,BICR 根据 RECIST1.1 确认的 ORR 为 51.6%(95%CI34.8%,68.0%);所有缓解患者均达到部分缓解。中位 DOR 为 5.4 个月(95%CI3.5%,NE)。队列 1 中 18 例中国患者接受本品推荐剂量 120 mg 每日一次治疗。中国亚组的有效性结果与全球有效性结果一致。
片剂
60mg
20°C至25°C(68°F至77°F),允许波动温度为15°C至30°C(59°F至86°F)。请储存于原包装容器中,以防潮。保持瓶盖紧闭。请勿取出干燥剂。开封后,请在3个月内用完。开封后3个月内丢弃所有未使用的药片。
国药准字HJ20250104

