轩菲宁说明书
Dirozalkib Tablets
地罗阿克
本品单药适用于未经过间变性淋巴瘤激酶(ALK)抑制剂治疗的 ALK 阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。
患者选择服用本品前,须获得经充分验证的检测方法证实的 ALK 阳性评估结果。推荐剂量本品的推荐剂量为 500 mg,口服给药,每日一次,与餐同服。连续服药,治疗直至疾病进展或出现不可耐受的毒性反应。应整片吞服,建议在每日相对固定的时间服用。若漏服或在服药后发生呕吐,无需补服本品,按照下次服药时间服用规定剂量即可。针对不良反应的剂量调整治疗过程中若出现不良反应,可能需要暂停用药、降低剂量或者停止本品的治疗,同时应根据患者耐受性,以每次减量 100 mg 的方式逐步降低本品的给药剂量。暂停本品治疗 3 周后,不良反应仍未能缓解的患者,应停止本品的治疗或遵医嘱。表 1 和表 2 为本品的一般剂量调整建议。
| 表1 地罗阿克剂量调整水平 | |
| 减量方案 | 剂量水平 |
| 标准剂量 | 500 mg,每日一次 |
| 第一次减量 | 400 mg,每日一次 |
| 第二次减量 | 300 mg,每日一次 |
表2 地罗阿克不良反应剂量调整建议
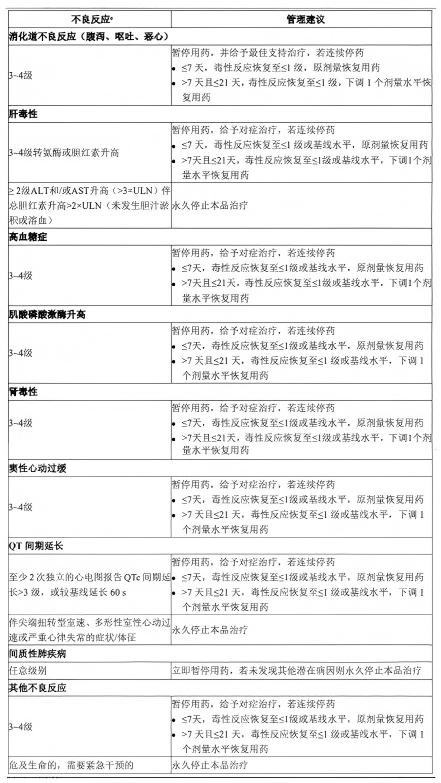
a,根据美国国家癌症研究所(NCI)不良事件通用术语标准(CTCAE)5.0 版进行分级。ULN = 正常值上限
与 CYP3A4 抑制剂或诱导剂联合使用
合并使用 CYP3A4 强抑制剂可导致本品暴露量升高,本品暴露量升高有导致毒性增加的风险。本品治疗期间应避免与 CYP3A4 强抑制剂合用。本品尚未开展与 CYP3A4 中效、弱效抑制剂的相互作用研究。合并使用 CYP3A4 强诱导剂可导致本品暴露量减少,本品暴露量减少有降低疗效的风险。本品治疗期间应避免与 CYP3A4 强诱导剂合用。本品尚未开展与 CYP3A4 中效、弱效诱导剂的相互作用研究。
特殊人群
肾功能不全患者
本品通过肾脏的消除可以忽略不计(仅 0.8% 的给药量从尿液排出),对于轻度(60 ≤ 肌酐清除率[CLcr]<90 mL/min)和中度肾功能不全(30 ≤ CLcr<60 mL/min)患者,无需剂量调整。重度肾功能不全(CLcr<30 mL/min)患者或终末期肾病患者慎用。
肝功能不全患者
轻度肝功能不全患者(总胆红素正常但天门冬氨酸氨基转移酶高于正常值上限,或总胆红素介于 1 倍至 1.5 倍的正常值上限)不推荐进行剂量调整。本品在中度肝功能不全患者(总胆红素介于 1.5 倍至 3 倍的正常值上限)中使用的数据量有限,尚无重度肝功能不全患者(总胆红素高于 3 倍的正常值上限)使用本品的数据。
本说明书描述了在临床试验中观察到的判断为可能由地罗阿克片引起的不良反应及其近似的发生率。由于每项临床试验的条件各不相同,在一个临床试验中观察到的不良反应的发生率不能与另一个临床试验观察到的不良反应发生率直接比较,也可能不能反映临床实践中的实际发生率。
地罗阿克片治疗晚期 NSCLC 的安全性数据来自 XZP-3621-1001 研究、XZP-3621-2001 研究和 XZP-3621-3001 研究的安全性汇总分析,共计 364 例晚期 NSCLC 患者接受地罗阿克片治疗,其中 325 例患者接受了地罗阿克片临床推荐剂量(500 mg)治疗。500 mg 剂量组中,地罗阿克片的中位暴露时间为 222 天,中位相对剂量强度为 98.6%,其中,15.7% 的患者因不良反应下调了地罗阿克片的剂量。
在 500 mg 剂量水平,地罗阿克片用于晚期 NSCLC 患者最常见的不良反应(发生率 ≥ 20%)包括腹泻、呕吐、恶心、丙氨酸氨基转移酶升高、天门冬氨酸氨基转移酶升高、体重降低、高尿酸血症、高甘油三酯血症、食欲减退、血肌酸磷酸激酶 MB 升高、贫血、高血糖症、血肌酐升高。严重程度 ≥ 3 级且发生率 ≥ 2% 的不良反应包括腹泻、γ-谷氨酰转移酶升高、高血糖症、高甘油三酯血症、心电图 QT 间期延长、低钾血症、ALT 升高、AST 升高、恶心、体重降低和贫血。导致暂停用药和剂量下调的最主要的不良反应为腹泻和呕吐。研究期间未发生导致死亡结局的不良反应。
地罗阿克片治疗后发生率 ≥ 5% 的不良反应详见表 3。
表3.地罗阿克片治疗后发生率≥5%的不良反应汇总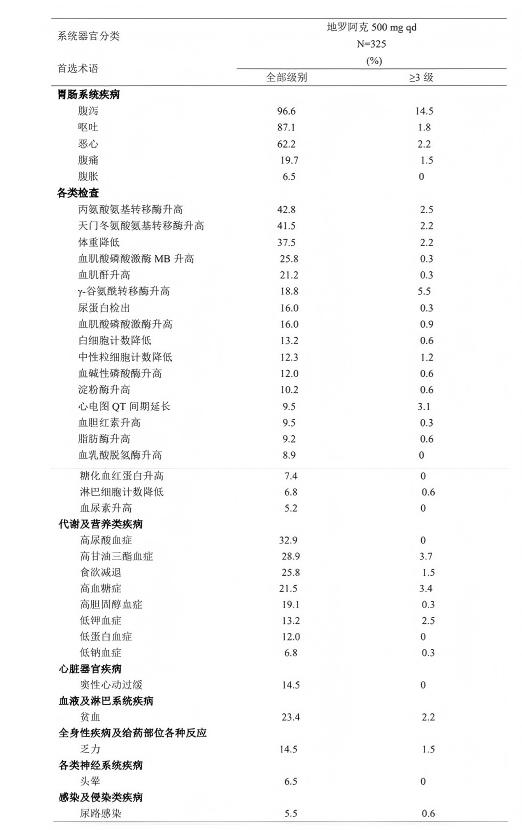
按照 MedDRA26.0 版列出系统器官分类和首选术语。
恶心:包括恶心和干呕。
腹痛:包括腹痛和上腹痛。
血肌酐升高:包括血肌酐升高和肾肌酐清除率降低。
尿蛋白检出:包括尿蛋白检出、蛋白尿和尿白蛋白检出。
中性粒细胞计数降低:包括中性粒细胞计数降低和中性粒细胞百分比降低。
高尿酸血症:包括高尿酸血症、血尿酸升高和痛风。
高甘油三酯血症:包括高甘油三酯血症和血甘油三酯升高。
高血糖症:包括高血糖症、血葡萄糖升高、糖尿病和 2 型糖尿病。
高胆固醇血症:包括高胆固醇血症、血胆固醇升高和低密度脂蛋白升高。
低钾血症:包括低钾血症和血钾降低。
低蛋白血症:包括低蛋白血症、白蛋白降低、总蛋白降低、血白蛋白降低、低白蛋白血症和前白蛋白降低。
窦性心动过缓:包括窦性心动过缓和心动过缓。
贫血:包括贫血、血红蛋白降低和红细胞计数下降。
乏力:包括乏力和疲劳。
特定不良反应描述
消化道反应
接受本品 500 mg 治疗的患者中,任何等级腹泻、呕吐和恶心的发生率分别为 96.6%、87.1% 和 62.2%,其中分别有 14.5%、1.8% 和 2.2% 的患者发生了 ≥ 3 级的腹泻、呕吐和恶心不良反应,0.9%、1.5% 和 0.6% 的患者发生了腹泻、呕吐和恶心严重不良反应,无致死性事件。腹泻、呕吐和恶心的中位开始时间分别为 1 天、1 天和 2 天,中位持续时间均为 2 天。96.5% 腹泻、98.6% 呕吐和 92.1% 恶心的患者结局为痊愈或好转。分别有 8.3%、5.2% 和 3.7% 的患者因腹泻、呕吐和恶心暂停治疗;4.0%、4.3% 和 2.2% 的患者因腹泻、呕吐和恶心下调剂量;0.3% 的患者因腹泻终止治疗,无患者因呕吐或恶心终止治疗。
肝毒性
接受本品 500 mg 治疗的患者中,任何等级丙氨酸氨基转移酶(ALT)升高和天门冬氨酸氨基转移酶(AST)升高的发生率分别为 42.8% 和 41.5%,其中分别有 2.5% 和 2.2% 的患者发生了 ≥ 3 级的 ALT 升高和 AST 升高不良反应,1.5% 和 1.2% 的患者发生了 ALT 升高和 AST 升高严重不良反应,无致死性事件。另有 3 例(0.9%)患者发生了 1-2 级肝功能异常不良反应,1 例(0.3%)患者发生了 3 级药物诱导的肝损伤,均未发生致死性事件。ALT 升高和 AST 升高的中位开始时间均为 29 天,中位持续时间均为 29 天。96.4%ALT 升高和 92.6%AST 升高的患者结局为痊愈或好转。分别有 0.6% 和 0.3% 的患者因 ALT 升高和 AST 升高暂停治疗;2.2% 和 1.5% 的患者因 ALT 升高和 AST 升高下调剂量;无患者因 ALT 升高和 AST 升高终止治疗。
肌酸磷酸激酶升高
接受本品 500 mg 治疗的患者中,任何等级肌酸磷酸激酶升高的发生率为 16.0%,其中 0.9% 的患者发生了 ≥ 3 级不良反应,仅 1 例(0.3%)患者发生了肌酸磷酸激酶升高的严重不良反应,无致死性事件。肌酸磷酸激酶升高的中位开始时间为 130.5 天,中位持续时间为 30 天。96.2% 肌酸磷酸激酶升高结局为痊愈或好转。分别有 1 例(0.3%)患者因肌酸磷酸激酶升高暂停治疗和下调剂量;无患者因肌酸磷酸激酶升高终止治疗。
窦性心动过缓
接受本品 500 mg 治疗的患者中,任何等级窦性心动过缓的发生率为 14.5%,未发生 ≥ 3 级窦性心动过缓不良反应,也未发生严重不良反应,无致死性事件。窦性心动过缓的中位开始时间为 29 天,中位持续时间也为 29 天。97.9% 窦性心动过缓的患者结局为痊愈或好转。仅 3 例(0.9%)患者因窦性心动过缓暂停治疗;无患者因窦性心动过缓下调剂量或终止治疗。
QT 间期延长
接受本品 500 mg 治疗的患者中,任何等级 QT 间期延长的发生率为 9.5%,其中 3.1% 的患者发生了 ≥ 3 级不良反应,未发生 QT 间期延长严重不良反应,无致死性事件。QT 间期延长的中位开始时间为 29 天,中位持续时间为 28 天。96.8%QT 间期延长的患者结局为痊愈或好转。有 1.8% 的患者因 QT 间期延长暂停治疗;仅 1 例(0.3%)患者因 QT 间期延长下调剂量;无患者因 QT 间期延长终止治疗。
肾毒性
接受本品 500 mg 治疗的患者中,任何等级血肌酐升高的发生率为 21.2%,仅 1 例(0.3%)患者发生了 ≥ 3 级不良反应,1 例(0.3%)患者发生血肌酐升高(2 级)严重不良反应,无致死性事件。另有 5.2% 的患者发生 1-2 级的血尿素升高,1.8% 的患者发生肾功能损害(其中 1 例为 3 级,其余均为 1-2 级),0.9% 的患者发生 1 级肾小球滤过率下降,均未发生致死性事件。血肌酐升高的中位开始时间为 26 天,中位持续时间为 29 天。所有血肌酐升高的患者均痊愈或好转。有 2 例(0.6%)患者因血肌酐升高暂停治疗;仅 1 例(0.3%)患者因血肌酐升高下调剂量;无患者因血肌酐升高终止治疗。
对本品活性成分或其中任何一种辅料过敏的患者禁用。
消化道反应
接受本品治疗的患者可能发生腹泻、呕吐和恶心等消化道不良反应。患者在服药前不需要使用预防性止吐药,建议服药后发生 ≥ 3 级胃肠道不良反应的患者及时就医,在医生指导下进行监测,并进行止泻、止吐和/或补液等支持性治疗。发生消化道不良反应的患者,应基于严重程度根据【用法用量】表 1 和表 2 进行剂量调整。
肝毒性
接受本品治疗的患者可能发生肝毒性。治疗前应进行肝功能检测,之后每月检测一次或遵医嘱。服药后出现转氨酶和/或胆红素升高患者,应在医师的指导下调整监测频率,并及时给予对症治疗。发生肝毒性的患者,应基于不良反应的严重程度根据【用法用量】表 1 和表 2 进行剂量调整。
肌酸磷酸激酶升
接受本品治疗的患者,可能会发生肌酸磷酸激酶 MB 升高、血肌酸磷酸激酶升高等不良反应。本品应尽量避免与能引起肌酸磷酸激酶升高的药物联用。患者在开始治疗前应进行肌酸磷酸激酶水平检查,治疗期间定期复查,出现肌酸磷酸激酶升高的患者,应在医师的指导下调整监测频率,并及时给予对症治疗。必要时,参照【用法用量】表 1 和表 2 对本品进行剂量调整。
窦性心动过缓
接受本品治疗的患者,可能会出现心动过缓。本品应尽量避免与其他已知可致心动过缓的药物(如β-受体阻滞剂、维拉帕米和地尔硫卓之类的非二氢吡啶类钙通道阻滞剂、可乐定及地高辛等)同时使用。治疗期间应定期监测心率和血压。如果患者发生症状性心动过缓,应对合并用药中已知可引发心动过缓的药物进行评估,并根据【用法用量】表 1 和表 2 进行剂量调整。
QT 间期延长
接受本品治疗的患者可能发生 QT 间期延长。先天性长 QT 综合征患者应避免使用本品。对于充血性心力衰竭、缓慢性心律失常、电解质异常或使用可延长 QT 间期药物的患者,应在服药前及服药过程中定期监测心电图及电解质,尤其在出现腹泻、呕吐、脱水或肾功能损害情况时。如患者发生 QT 间期延长,应对合并用药中已知可引发 QT 间期延长的药物进行评估,并根据【用法用量】表 1 和表 2 进行剂量调整。
肾毒性
接受本品治疗的患者可能发生肾功能损害。推荐患者在治疗前进行血肌酐、肌酐清除率等肾功能指标监测,治疗期间每个月监测一次或遵医嘱,有肾功能损害危险因素或既往病史的患者可缩短监测周期。尚未在肾功能不全患者中开展临床试验,中度或重度肾功能不全的患者应在医师指导下慎用本品。发生肾功能受损的患者,应基于严重程度根据【用法用量】表 1 和表 2 进行剂量调整。
高血糖症
接受本品治疗的患者可发生高血糖症(详见【不良反应】)。糖尿病和/或高血糖未得到充分控制的患者发生高血糖症的风险可能会增加。在开始使用本品前,应检测血糖相关指标,在治疗第 1 周期每 2 周监测 1 次,后续每周期监测 1 次或根据临床情况进行监测。对于出现严重(3 级或 4 级)反应的患者应暂停用药和/或剂量调整(参见【用法用量】),实施或优化降血糖治疗等措施,加强监测频率,并完善检查,鉴别导致高血糖的其它原因。
间质性肺疾病(ILD)
接受本品治疗的患者研究期间未发生 ILD 不良反应,参考同类已上市产品,若患者出现提示 ILD/非感染性肺炎的肺部症状急性发作和/或不明原因加重(如呼吸困难,可伴有咳嗽和低热,X 线胸片示弥漫阴影,低氧血症)时,应立即就医,并监测肺部症状。如果怀疑为 ILD/非感染性肺炎,应暂停本品治疗,并根据症状体征考虑吸氧、抗炎和抗生素等对症支持治疗。如果没有发现其他 ILD/非感染性肺炎的潜在病因,应永久停用本品治疗。
与 CYP3A4 抑制剂或诱导剂联合使用
合并使用 CYP3A4 强抑制剂可导致本品暴露量升高,CYP3A4 中等抑制剂可能增加本品的暴露量,本品暴露量升高有导致毒性增加的风险。本品治疗期间应避免与强效 CYP3A4 抑制剂合用。当停止给予强效 CYP3A4 抑制剂且至该药物清除 3-5 个半衰期后,恢复使用强效 CYP3A4 抑制剂之前本品的用药剂量。如合并使用 CYP3A4 中等抑制剂,应密切监测不良反应。
合并使用 CYP3A4 强诱导剂可导致本品暴露量减少,本品暴露量减少有降低疗效的风险。应避免本品与 CYP3A4 强诱导剂合用。
86983872000036,86983872000043
地罗阿克为间变性淋巴瘤激酶(ALK)抑制剂,体外对 ALK 活性的半数抑制浓度(IC50)为 0.21nM,对耐药突变型 ALK(L1196M 或 G1202R)的 IC50分别为 0.29 和 0.92nM。地罗阿克对 ROS1 活性具有一定抑制作用,IC50为 0.41nM,对耐药突变型 ROS1(G2032R)的 IC50为 2.17nM。在小鼠异种移植瘤模型中,地罗阿克可抑制携带 ALK 融合及其突变基因的肿瘤和病人来源异种移植(PDX)肿瘤的生长,在小鼠颅内移植瘤模型中也可见抗肿瘤活性。
遗传毒性
地罗阿克的 Ames 试验、中国仓鼠卵巢细胞体外染色体畸变试验和大鼠体内骨髓细胞微核试验结果均为阴性。
生殖毒性
地罗阿克尚未开展生育力和早期胚胎发育试验。
在大鼠胚胎-胎仔发育毒性试验中,妊娠大鼠于器官发生期(妊娠第 6-17 天)每天 1 次经口给予地罗阿克 10、30 或 100 mg/kg/天, ≥ 30 mg/kg/天(以暴露量计,约为人推荐剂量 500 mg/天的 0.33 倍)剂量下可见母体体重和摄食量降低,100 mg/kg/天(以暴露量计,约为人推荐剂量 500 mg/天的 0.67 倍)剂量下还可见母体异常临床表现(如消瘦、活动减少、背部弓起和毛发蓬乱等),所有剂量下均未见胚胎-胎仔发育毒性。
在兔胚胎-胎仔发育毒性试验中,妊娠兔于器官发生期(妊娠第 6-19 天)每天 1 次经口给予地罗阿克 6、12 或 25 mg/kg/天, ≥ 12 mg/kg/天(以暴露量计,约为人推荐剂量 500 mg/天的 0.40 倍)剂量下可见母体动物死亡,存活动物可见摄食量下降、粪便较少,25 mg/kg/天(以 AUC 计,约为人推荐剂量 500 mg/天的 0.74 倍)剂量下可见母体体重、摄食量降低,妊娠子宫重降低和妊娠期增重降低, ≥ 12 mg/kg/天剂量下可见平均胎仔体重和体长比下降,早期吸收胎数量升高引起的活胎仔数下降,胚胎-胎仔死亡总数和着床后丢失率升高,25 mg/kg 剂量组下可见平均胎仔体重下降,对母体毒性及胚胎-胎仔发育毒性的 NOAEL 为 6 mg/kg/天。
致癌性
地罗阿克尚未进行致癌性试验。
吸收
患者单次口服地罗阿克片,血药浓度约 3.0 h-4.0 h 达峰值,50 mg-600 mg 剂量范围内 Cmax和 AUC 随剂量增加不呈线性。与餐同服条件下,患者每天一次口服地罗阿克片 500 mg,血药浓度第 8 天达稳态,AUC 和 Cmax蓄积指数的几何均值分别为 1.086 和 0.969,表明多次给药无明显蓄积。
食物影响
一项健康受试者单次口服地罗阿克片 400 mg 的食物影响临床研究显示,与空腹给药相比,受试者高脂餐(总热量约 1000Kcal,其中脂肪供能占比约 50%)或标准餐(总热量约 500Kcal,其中脂肪供能占比约 25%)后口服地罗阿克片 AUC0-t分别增加约 22.68% 和 64.22%(几何均值比),Cmax分别增加 43.15% 和 82.46%(几何均值比),食物可增加药物的生物利用度。标准餐后给药,Tmax较空腹给药提前约 1 h,而高脂餐后给药与空腹给药 Tmax一致。
分布
地罗阿克与人血浆蛋白的结合率约为 95%。与餐同服条件下,患者单次口服地罗阿克片 500 mg 的表观分布容积(Vd/F)的几何均值约为 5609L。地罗阿克及相关物质与血细胞有结合,在全血与血浆中浓度的比值在 1.25-1.86 之间。
消除
与餐同服条件下,患者单次口服地罗阿克片 500 mg 的血浆药物浓度半衰期的几何均值为 23 h。地罗阿克片 500 mg 单次给药和多次给药的表观清除率(CL/F)分别为 164L/h 和 276L/h。
代谢
体外研究显示地罗阿克主要经过 CYP3A4 代谢。餐后条件下,健康受试者单次口服放射性标记的地罗阿克 400 mg,原形药地罗阿克是血浆中的主要药物成分(96.98%)。血浆中共检出 5 种代谢产物,其中浓度最高的代谢物占血浆总放射性暴露量的 3.02%,其余代谢物含量极低,无法准确定量。地罗阿克在男性健康受试者体内主要的代谢途径为:(1)单氧化;(2)脱异丙基及进一步的氧化;(3)N-脱烷基及进一步的氧化或葡萄糖醛酸结合等。
排泄
餐后条件下,健康受试者单次口服放射性标记的地罗阿克 400 mg,尿液和粪便中的总放射性回收率(% 给药量)为 96.84%,主要从粪便中排出(96.05%),粪便中原型药物是主要成分,占给药量的 67.53%;仅微量从尿液中排出(0.80%)。
特殊人群
年龄、性别和体重的影响
一项群体药代动力学结果显示年龄、性别、体重均非具有临床意义的协变量。
肾功能不全患者
一项包括 241 例肾功能正常( ≥ 90 mL/min)、188 例轻度肾功能不全(60 ≤ CLcr<90 mL/min)和 12 例中度肾功能不全(30 ≤ CLcr<60 mL/min)患者的群体药代动力学分析显示,肾功能正常与轻度肾功能不全患者之间的暴露分布相当,中度肾功能不全患者的暴露略高于上述两人群,但暴露分布仍有较大重叠,同时考虑到仅 0.8% 的给药量从尿液排出,即肾脏不是主要排泄器官,因此对于轻度和中度肾功能不全患者,无需剂量调整。重度肾功能不全的样本量非常有限;尚无终末期肾病患者数据,建议重度肾功能不全患者或终末期肾病患者慎用本品。
肝功能不全患者
一项包括 384 例肝功能正常(总胆红素和天门冬氨酸氨基转移酶均低于正常值上限)和 60 例轻度肝功能不全(总胆红素正常但天门冬氨酸氨基转移酶高于正常值上限,或总胆红素介于 1 倍至 1.5 倍的正常值上限)患者的群体药代动力学分析显示,轻度肝功能不全和肝功能正常患者之间的暴露相当,无需剂量调整。中度肝功能不全(总胆红素介于 1.5 倍至 3 倍的正常值上限)的样本量非常有限;尚无重度肝功能不全(总胆红素高于 3 倍的正常值上限)患者数据。
国药准字H20250055,国药准字H20250056

