唯铭赞说明书
Elosulfase Alfa Injection
依洛硫酸酯酶α
活性成分:Elosulfase alfa是利用重组DNA技术由中国仓鼠卵巢(CHO)细胞表达制备的重组人N-乙酰半乳糖胺-6-硫酸酯酶(rhGALNS)。
辅料:
醋酸钠三水合物 磷酸二氢钠一水合物
L-精氨酸盐酸盐
山梨醇
聚山梨酯20
注射用水
本品适用于IVA型黏多糖贮积症患者(MPS IVA,Morquio A综合征)。
应在有MPSIVA或其他遗传代谢疾病经验的医生监督下进行本品治疗。应由经过适当培训并且有能力处理紧急医学情况的的医护人员进行本品的给药。肝肾功能不全患者:Vimzim治疗的严重肝和/或肾功能不全患者的安全性和临床经验有限。对这些患者的使用应考虑进行细心的管理和观察。剂量:本品的建议剂量为2mg/kg体重,每周给药一次。输注的总体积约在4小时以上给药完毕(见表1)。在治疗前给予抗组胺药,伴或不伴退热剂,建议在输注开始前30~60分钟使用。给药方法:仅供静脉输注使用。体重小于25kg的患者将接受总体积100ml的输注。如果稀释于100mL,则起始输注速率应为3mL/小时。如果耐受良好可以每15分钟增加输注速率,具体如下:第一次将速率增至6mL/小时,然后每15分钟增加6mL/小时直到达到最大速率36mL/小时。体重为25kg或者以上的患者将接受总体积250mL的输注。如果稀释于250mL,则起始速率应为6mL/小时。如果耐受良好可以每15分钟增加输注速率,具体如下:第一次将速率增至12mL/小时,然后每15分钟增加12mL/小时直到达到最大速率72mL/小时。表1:推荐输注的体积和速率
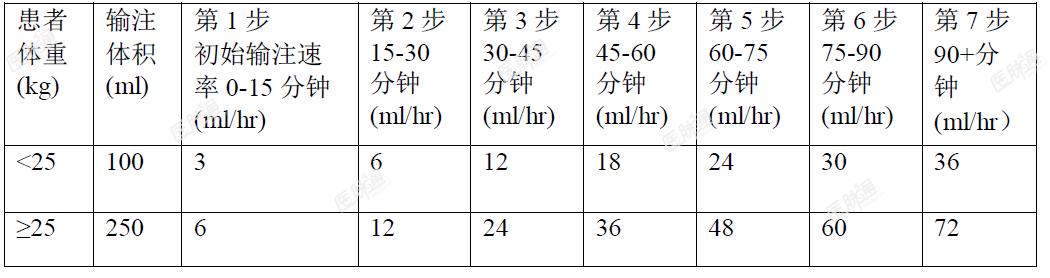
*输注速率依据患者的耐受程度而增加。每瓶Vimizim仅用于一次性使用。必须用9mg/ml(0.9%)氯化钠溶液稀释Vimizim,以便使用无菌技术进行输液。稀释后的溶液用输液器给病人注射。可使用配有低蛋白结合的0.2pm直插式过滤器的输液器。未使用过的药品或废料应按照当地要求处理。Vimizim输液的制备:采用无菌技术。给药前必须稀释Vimizim。要稀释的药瓶数量是根据患者的体重而定的。建议剂量为2mg/kg。1.根据单个患者的体重和推荐剂量2mg/kg确定要稀释的小瓶数量,2.计算方法如下:患者体重(kg)乘以2(mg/kg)=患者剂量(mg),患者剂量(mg)除以1(mg/mlVimizim浓缩物)=ml Vimizim总量,总量(ml)Vimizim除以每小瓶5ml=小瓶总数,2.计算出的小瓶总数四舍五入到下一整瓶。从冰箱中取出适当数量的小瓶。不要加热或微波瓶。不要摇晃瓶子。3.含有静脉注射的氯化钠9mg/ml(0.9%)输液袋适用静脉给药。输液总量由患者体重决定。体重小于25kg的患者应接受100ml的总体积。体重大于等于25kg的患者应接受250ml的总体积。4.在从小瓶中取出Vimizim之前,目视检查每个小瓶是否有颗粒物和变色。因为这是一种蛋白质溶液,可能会发生轻微的絮凝(半透明纤维)。Vimizim溶液应澄清至略带乳光,无色至淡黄色。如果溶液变色或溶液中有微粒物质,请勿使用。
5.从输液袋中取出和丢弃9mg/ml(0.9%)氯化钠溶液,其体积等于添加的Vimizim浓缩液的体积。6. 从适当数量的小瓶中计算出的Vimizim体积慢慢地取出,小心避免过度搅动。7. 慢慢地将Vimizim添加到输液袋中,小心避免搅拌。8. 轻轻旋转输液袋,确保Vimizim的正确分布。不要摇晃溶液。9. 稀释后的溶液用输液器给病人注射。可使用配有0.2微米直插式过滤器的输液器。
不良反应的评价基于176例年龄为5~57岁的MPSIVA患者在一项随机、双盲、安慰剂对照试验中的暴露经验,患者接受2mg/kg本品每周一次给药(n=58),2mg/kg本品隔周给药一次(n=59)或安慰剂(n=59)。临床试验中的大多数不良反应是IRs,定义为在开始输液后直到输液后一天结束时发生的反应。临床试验中观察到严重的IRs,包括过敏反应、超敏反应和呕吐。IRs最常见的症状是头痛、恶心、呕吐、发热、寒战和腹痛(在接受Vimizim治疗的患者中,出现率≥10%,与安慰剂相比,出现率≥5%)oIRS一般为轻度或中度,治疗前12周的频率较高,随着时间的推移,发病率往往较低。不良反应列表:下表2中的数据描述了Vimizim治疗患者临床试验的不良反应。频率定义为:十分常见(≥1/10)、常见(≥1/100至<1/10)、偶见(≥1/1000至<1/100)、罕见(≥1/10000至<1/1000)、十分罕见(<1/10000)且未知(无法根据可用数据进行估计)。在每个频率分组中,不良反应按严重性降低的顺序出现。表2:Vimizim治疗患者的不良反应
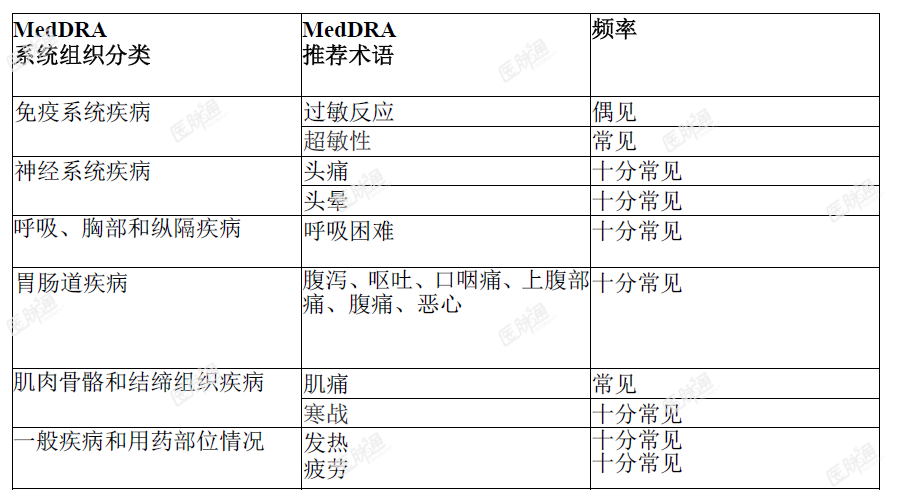
免疫原性:所有接受本品治疗的患者均产生持续的抗药抗体,大约80%的患者可以中和抗体,该抗体对能够抑制药物结合至非阳离子依赖型甘露糖-6-磷酸受体。尽管出现了抗依洛硫酸酯酶a抗体,但在各项试验中仍观察到疗效指标的持续改善和尿硫酸角质素(KS)的降低。尚不能确定抗体效价较高或中和抗体阳性与疗效指标的降低或出现过敏反应或其他超敏反应之间的相关性。在接受治疗的患者中≤10%检测出抗依洛硫酸酯酶a的IgE抗体,与过敏反应或其他超敏反应和/或停药并无一致的相关性。
对活性物质或列于成份项下的任何辅料具有危及生命的超敏反应 (过敏反应)
警告:过敏风险:在 Vimizim 输注过程中一些患者出现了危及生命的过敏反应。无论治疗过程的持续时间如何,已报告的在Vimizim输注期间发生过敏反应,表现为咳嗽、红斑、喉部紧绷、荨麻疹、潮红、紫绀、低血压、皮疹、呼吸困难、胸部不适和胃肠道症状(如恶心、腹痛、干呕和呕吐),与荨麻疹有关。密切观察 Vimizim 给药期间和给药后的患者,并做好管理过敏反应的准备。将过敏反应的体征和症状告知患者,并在出现症状时立即就医。急性呼吸系统疾病患者可能因过敏反应而面临严重呼吸衰竭的急性加重的风险,需要进行额外的监测
过敏反应和严重的变态反应:Vimizim治疗的患者有过敏反应和超敏反应。在上市前的临床试验中,235例(7.7%)Vimizim治疗的患者中有18例出现与过敏反应一致的体征和症状。这18名患者在输液过程中出现26种过敏反应,症状包括咳嗽、红斑、喉部紧绷、荨麻疹、潮红、紫绀、低血压、皮疹、呼吸困难、胸部不适和胃肠道症状(如恶心、腹痛、干呕和呕吐)以及荨麻疹。这些过敏性病例最早发生在输液开始后30分钟和输液后3小时。到第47次输注时,过敏反应最迟出现在治疗过程中。在Vimizim的临床试验中,235名患者中有44名(18.7%)出现过敏反应,包括过敏反应。超敏反应最早发生在输液开始后30分钟,最迟发生在输液后6天。过敏反应的常见症状(发生在2名以上患者中)包括过敏反应、荨麻疹、周围水肿、咳嗽、呼吸困难和潮红。
由于可能出现过敏反应,因此在注射Vimizim时应随时提供适当的医疗支持。考虑到上市前临床试验中出现过敏反应的时间,在服用Vimizim后密切观察患者一段适当的时间。将过敏反应的体征和症状告知患者,并指示他们在出现体征和症状时立即就医。由于可能发生过敏反应,在输注前服用抗组胺药,无论是否服用退热药。过敏反应的处理应根据反应的严重程度,包括缓慢或暂时中断输注和/或额外服用抗组胺药、退热药和/或皮质类固醇以治疗轻微反应。然而,如果出现严重的过敏反应,立即停止注射本品并开始适当的治疗。考虑重新服用Vimizim后的严重不良反应风险和益处。输液反应:输液反应(IR)定义为在开始输注后到输注后次日结束前发生的反应。IR是在临床研究中接受本品治疗的患者中最常见的不良反应。IR可能包括变态反应[见过敏反应和严重变态反应]。在临床研究中观察到的严重IR包括过敏反应、超敏反应和呕吐。最常见的IR症状(在≥10%接受本品治疗的患者中发生并且发生率与安慰剂相比≥5%)有头痛、恶心、呕吐、发热、寒战和腹痛。IR通常为轻度或中度,在治疗的前12周的发生率较高,倾向于随时间减少。因为本品潜在的IR,患者在输注前应给予抗组胺药伴/不伴退热药。IR的处理应根据反应的严重程度和包括减慢或暂时中断输注和/或给予额外的抗组胺药、退热药,和/或皮质类固醇;对于某些发生IR的患者,后续输注需要降低输注速率以及使用额外的预防药物。如果发生严重的IR,应立即停止本品输注并且采取适当的治疗。发生重度反应后应考虑再次给予本品的风险和获益。急性呼吸系统并发症的风险:Vimizim输注时患有急性发热或呼吸系统疾病的患者可能因过敏反应而面临危及生命的并发症。在注射Vimizim之前,应仔细考虑患者的临床状况,并考虑推迟Vimizim的输注。睡眠呼吸暂停在MPSIVA患者中很常见。在开始Vimizim治疗前,应考虑评估气道通畅性。在睡眠期间使用补充氧气或持续气道正压通气(CPAP)的患者在输液期间,如果出现急性反应,或使用抗组胺药导致极度困倦/睡眠,应立即接受这些治疗。脊髓或颈脊髓压迫:脊髓或颈脊髓压迫(SCC)是MPSIVA已知的严重并发症,可能作为疾病自然史的部分发生。在临床试验中,在接受本品治疗患者和接受安慰剂治疗患者都有观察到SCC。MPSIVA患者应监视SCC的体征和症状(包括背痛、压迫水平以下肢体麻痹、大小便失禁)和给予适当临床护理。山梨醇(E420):本品每小瓶含有100毫克山梨醇,相当于40毫克/千克。患有遗传性果糖不耐症(HFI)的患者,除非严格必要,否则不得服用该药物。婴儿和幼儿(2岁以下)可能尚未被诊断为遗传性果糖不耐症(HFI)。静脉注射含有山梨醇/果糖的药物可能危及生命。在治疗前,必须对儿童的治疗益处与相关风险进行全面评估。在给每位患者服用该药物之前,必须对其进行详细的HFI症状史研究。免疫原性:预测本品给药会导致抗体产生,因此,最好是定期进行对重组人N-乙酰半乳糖胺-6-硫酸酯酶(基因重组)的抗体检查。对驾驶或机械操作能力的影响:Vimizim对驾驶和操作机械能力影响小。有报道在输注本品时发生头晕,若输注后发现头晕,可能会影响驾驶和操作机械的能力。没有进行本品对驾驶或机械操作能力影响方面的研究
在临床试验中没有药物过量的经验。
在儿童人群中的剂量与成人相同。Vimizim的安全性和有效性已在5岁及以上的儿童患者中得到证实。对不满5岁儿童的用药经验不足,在一项开放性试 中15例MPS IVA儿童患者的年龄在5岁以下(9个月〜<5岁),接受2 mg/kg 本品每周一次共52周。
C级:
尚未进行相互作用的研究。
Vetter Pharma-Fertigung GmbH & Co.KG
86980775000019
临床研究数据/药效学性质:本品的临床试验评价治疗对于MPSIVA各方面的全身表现的影响,包括耐性、呼吸功能、生长速度、活动能力和尿KS。在6项临床试验中总共有235例MPSIVA患者入组并暴露于本品。176例5~57岁的MPSIVA患者在一项随机,双盲,安慰剂对照3期临床试验中,评估本品的安全性和疗效。大部分患者存在身材矮小、耐力受损以及肌肉骨骼症状。所有纳入试验的患者在基线时的6分钟步行测试(MWT)距离超过30m但少于325m。患者接受本品2mg/kg每周一次(n=58)或2mg/kg隔周一次(n=59)或安慰剂(n=59)治疗,总共24周。所有患者在每次输注前均接受抗组胺药治疗。主要终点是第24周时6MWT距离相对于基线的变化,与安慰剂进行比较。次要终点是第24周时的3分钟爬梯测试(MSCT)以及尿KS水平相对于基线的变化。总共173例患者进入了扩展期试验,在此期间患者接受本品2mg/kg每周一次或2mg/kg隔周一次,在得到第24周结果后全部转为2mg/kg每周一次治疗。在第24周时评价主要和次要终点。2mg/kg/周与安慰剂相比,6分钟步行距离的模型疗效为22.5m(CI95,4.0,40.9;p=0.0174)。2mg/kg/周方案与安慰剂相比,每分钟爬梯的模型疗效为1.1阶/分钟(CI95,-2.1,4.4;p=0.4935)。2mg/kg/周与安慰剂相比,尿KS的百分比变化的模型疗效为-40.7%(CI95,-49.0,-32.4;p<0.0001)。安慰剂组和每周一次治疗组对于所有终点的差异最大。隔周一次方案的6分钟步行距离和每分钟爬梯阶数与安慰剂相近。表:2mg/kg/周的安慰剂对照临床研究的结果
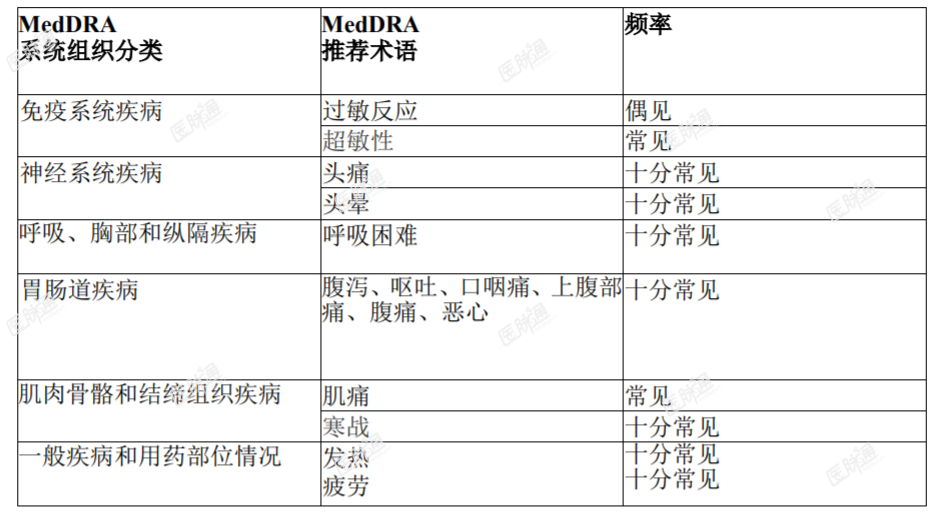
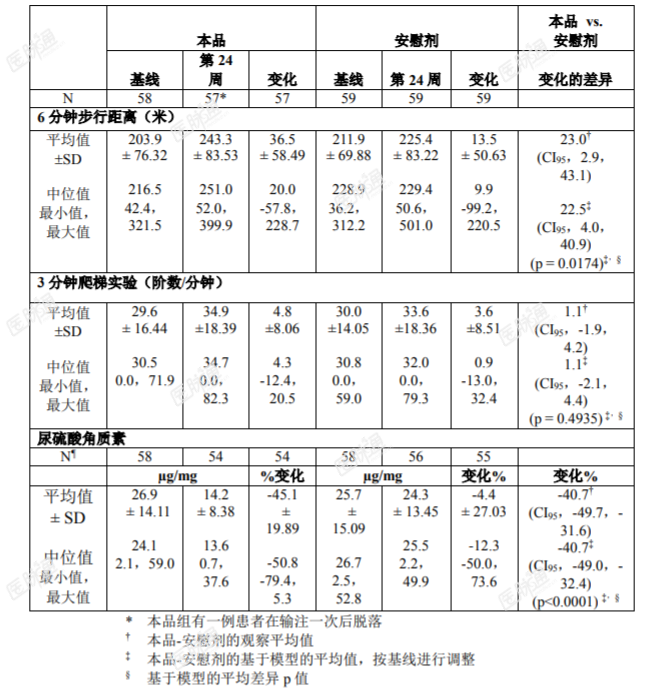
*本品纟 且有一例患者在输注一次后脱落,本品-安慰剂的观察平均值,本品-安慰剂的基于模型的平均值,按基线进行调整§基于模型的平均差异p值,未获得所有入组患者的结果,在另一项延长期试验中,患者接受本品2mg/kg/周,显示最初获得的耐力的改善以及尿KS的持续降低可以保持到第156周。
注射剂
每瓶5mL,含依洛硫酸酯酶α5mg(1mg/ml)。
透明玻璃瓶(I型)配丁基橡胶塞,易拉铝塑组合盖。 包装规格:1瓶/盒
2-8℃冰箱储存。 请勿冷冻。 避光保存。
30.00
36个月稀释后:已证实在2C~8C放置24小时随后在23 C ~27 C放置24小时的化学和物理使用稳定性。 从微生物学安全性的角度,稀释后的溶液应当立即使用。如果未能立即使用, 应由使用者对临床使用
S20190024

