PAXLOVID说明书
nirmatrelvir and ritonavir
利托那韦
奈玛特韦
奈玛特韦活性成分的化学名称为(1R,2S,5S)-N-((1S)-1-氰基-2-((3S)-2-氧代吡咯烷-3-基)乙基)-3-((2S)-3,3-二甲基-2-(2,2,2-三氟乙酰胺基)丁酰基)-6,6-二甲基-3-氮杂双环[3.1.0]己烷-2-甲酰胺]。分子式为C23H32F3N5O4,分子量为499.54。奈玛特韦的结构式如下: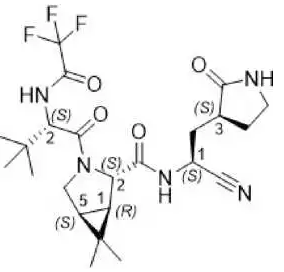
奈玛特韦供应为速释薄膜衣片。每片含150mg 奈玛特韦 和以下非活性成分:胶态二氧化硅、交联羧甲基纤维素钠、乳糖一水合物、微晶纤维素和硬脂富马酸钠。以下为薄膜包衣的成分:羟丙基甲基纤维素、氧化铁红、聚乙二醇和二氧化钛。
利托那韦
利托那韦的化学名称为10-羟基-2-甲基-5-(1-甲基乙基)-1-[2-(1甲基乙基)-4-噻唑基]-3,6-二氧代-8,11-双(苯基甲基)-2,4,7,12-四氮杂十三烷-13-酸,5-噻唑基甲酯,[5S-(5R*,8R*,10R*,11R*)]。其分子式为C37H48N6O5S2,分子量为720.95。利托那韦的结构式如下: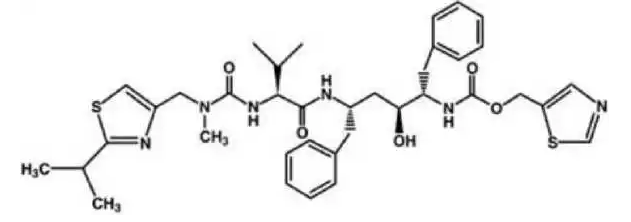
利托那韦供应为薄膜衣片。每片含100mg 利托那韦和以下非活性成分:无水磷酸氢钙、胶态二氧化硅、共聚维酮、硬脂酰富马酸钠和山梨糖醇单月桂酸酯。以下为薄膜包衣的成分:胶态二氧化硅、羟丙基纤维素、羟丙甲纤维素、聚乙二醇400、聚乙二醇3350、聚山梨醇酯80、滑石粉和二氧化钛。
奈玛特韦为粉色的椭圆形速释薄膜衣片,一面凹刻有“PFE”,另一面刻有“3CL”。 利托那韦为白色椭圆形薄膜衣片,凹刻有“a”标志和代码NK。
PAXLOVID未被授权用于因重度或危重COVID-19并需要住院的患者的初始治疗。
PAXLOVID未被授权用于预防COVID-19的暴露前或暴露后预防。
PAXLOVID未被授权连续使用超过5天。
PAXLOVID只能由根据国家法律获得许可或授权处方PAXLOVID所属治疗类别药物(即抗感染药)的医生、高级执业注册护士和医生助理为个体患者处方。
PAXLOVID未被批准用于任何用途,包括用于治疗COVID-19。
针对中度肾损害(eGFR≥30至<60 mL/min)降低剂量:150 mg 奈玛特韦(一片150 mg片剂)和100 mg利托那韦(一片100 mg片剂),两片片剂一起服用,每日两次,持续5天。
不建议PAXLOVID用于重度肾损害患者(eGFR <30 mL/min)。
不建议PAXLOVID用于重度肝损害患者(Child-Pugh C级)。
PAXLOVID紧急使用剂量
奈玛特韦必须与利托那韦联合给药。奈玛特韦与利托那韦未能正确联合给药可能导致奈玛特韦的血浆水平不足以达到预期的治疗效果。
PAXLOVID的剂量为300 mg 奈玛特韦(两片150 mg片剂)和100 mg利托那韦(一片100 mg片剂),三片片剂一起服用,每日两次,持续5天。处方应指定PAXLOVID中每种活性成分的数字剂量。根据公共卫生建议完成完整的5天疗程和持续隔离对于最大化病毒清除和最小化SARS-CoV-2传播非常重要。
PAXLOVID的5天疗程应在诊断为COVID-19后尽快开始,并在症状发作后5天内开始。如果患者在开始PAXLOVID治疗后因重度或危重COVID-19需要住院,应根据医疗人员的判断完成完整的5天疗程。
如果患者在通常服药后8小时内漏服一剂PAXLOVID,患者应尽快服用,并恢复正常给药方案。如果患者漏服一剂药物的时间超过8小时,则患者不应服用漏服的剂量,而应在常规计划时间服用下一剂药物。患者不应为了弥补漏服的剂量而将剂量加倍。
PAXLOVID(奈玛特韦和利托那韦片剂)可与或不与食物同服 [参见 临床药理学]。整片吞服,不可咀嚼、分片或压碎。
2.2肾损害患者的重要给药信息
对轻度肾损害患者(eGFR ≥60 至 <90 mL/min)无需调整剂量。在中度肾损害(eGFR≥30至<60 mL/min)患者中,PAXLOVID的剂量为150 mg 奈玛特韦和100 mg利托那韦,每日两次,持续5天。处方应指定PAXLOVID中每种活性成分的数字剂量。医疗人员应向患者告知肾病患者用药指导[参见 患者须知信息]。
在获得更多的可用数据之前,暂不建议PAXLOVID用于重度肾损害患者(eGFR <30 mL/min);尚未确定重度肾损害患者的适当剂量[参见 特殊人群用药和 临床药理学]。
2.3肝损害患者用药
对轻度(Child-Pugh A级)或中度(Child-Pugh B级)肝损害患者无需调整剂量。尚未获得重度肝损害(Child-Pugh C级)受试者使用奈玛特韦或利托那韦的药代动力学或安全性数据;因此,不建议重度肝损害患者使用PAXLOVID[参见 特殊人群用药]。
2.4与PAXLOVID的重要药物相互作用
与其他含利托那韦或可比司他的产品合用时无需调整剂量。
接受含利托那韦或可比司他的HIV或HCV治疗方案的患者应根据指征继续接受治疗。
与PAXLOVID的重要药物相互作用见本情况说明书的其他章节。考虑PAXLOVID治疗前和治疗期间发生药物相互作用的可能性,并审查PAXLOVID治疗期间的合并用药[参见 禁忌症,警告与注意事项和药物相互作用]。
不良事件(发生率≥1%且差异≥5例受试者)包括味觉障碍、腹泻、高血压和肌痛。
PAXLOVID 禁用于对其活性成分(奈玛特韦或利托那韦)或本品中任何其他成分具有临床意义超敏反应史[如,中毒性表皮坏死松解症(TEN) 或 Stevens-Johnson 综合征]的患者。
PAXLOVID禁止与清除高度依赖于CYP3A且浓度升高可致严重和/或危及生命反应的药物合用[参见 药物相互作用]
PAXLOVID 禁止与强效CYP3A 诱导剂合用,奈玛特韦或利托那韦血浆浓度显著降低可能与潜在的病毒学反应丧失和可能的耐药性相关。由于近期停用的CYP3A 诱导剂的失效会延迟,因此,在停用以下任何药物后不能立即开始使用PAXLOVID [参见 药物相互作用]
PAXLOVID与某些其他药物同时使用可能会导致潜在显著的药物相互作用。在治疗前以及治疗期间应咨询有关潜在药物相互作用的完整处方信息。
肝脏毒性:接受利托那韦治疗的患者曾发生肝转氨酶升高、临床肝炎和黄疸。
HIV-1耐药性:在HIV-1感染未得到控制或未确诊的个体中,使用PAXLOVID可能导致HIV-1对HIV蛋白酶抑制剂产生耐药性的风险。
除非授权被提前终止或撤销,否则根据法案第564(b)(1)节,21 U.S.C.§360bbb-3(b)(1),PAXLOVID仅在声明(存在证明授权紧急使用PAXLOVID是合理的情况)的持续期内获得授权使用。
COVID-19大流行期间紧急使用药物的理由、可用替代药物的信息和COVID-19的其他信息见医疗人员的完整情况说明书。
合用PAXLOVID可改变其他药物的血浆浓度,其他药物也可能改变PAXLOVID的血浆浓度。考虑PAXLOVID治疗前和治疗期间发生药物相互作用的可能性,并审查PAXLOVID治疗期间的合并用药。
Pfizer Inc
奈玛特韦是SARS-CoV-2主要蛋白酶(Mpro)的拟肽抑制剂,也称为3C样蛋白酶(3CLpro)或nsp5蛋白酶。SARS-CoV-2 Mpro的抑制使其不能加工多聚蛋白前体,阻止病毒复制。在生化试验中,奈玛特韦可抑制重组SARS-CoV-2 Mpro的活性,Ki值为3.1 nM,IC50值为19.2 nM。通过X射线晶体学发现奈玛特韦与SARS-CoV-2 Mpro活性位点直接结合。
利托那韦是一种HIV-1蛋白酶抑制剂,但对SARS-CoV-2 Mpro无活性。利托那韦抑制CYP3A介导的奈玛特韦代谢,导致奈玛特韦血浆浓度升高。
已在健康受试者中研究了奈玛特韦/利托那韦的药代动力学。
利托那韦作为一种药代动力学增强剂与奈玛特韦联合给药,导致奈玛特韦的全身浓度更高,半衰期更长,从而支持每日两次给药方案。
口服奈玛特韦/利托那韦后,单次给药剂量高达750 mg和多次给药剂量高达500 mg每日两次时,全身暴露量的增加比例似乎低于剂量比例。10天内每日两次给药在第2天达到稳态,蓄积率约2倍。奈玛特韦/利托那韦的药代动力学特性见表2。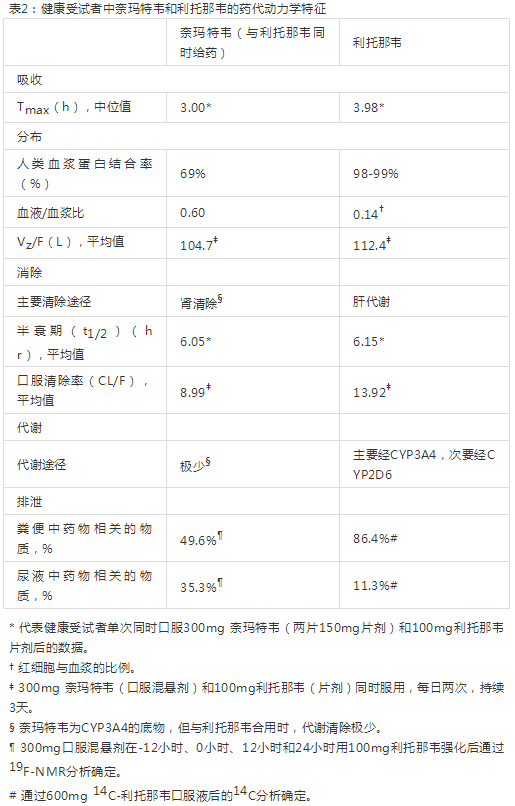
健康受试者单次口服PAXLOVID 的药代动力学数据描述如下(表3)。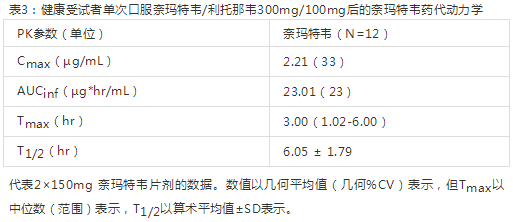
食物对奈玛特韦口服吸收的影响
与空腹状态相比,奈玛特韦混悬剂与利托那韦片剂联合给药后,与高脂餐同服适度增加了奈玛特韦的暴露量(平均Cmax增加约15%,平均AUClast增加约1.6%)。
复合包装
奈玛特韦150 mg;利托那韦100 mg
在USP控制的室温20°C至25°C(68°F至77°F)下储存;允许在15°C到30°C(59°F到86°F)之间进行偏移。

