福甘定说明书
Tenofovir Disoproxil Fumarate Capsules
替诺福韦
本品主要成份为富马酸替诺福韦二吡呋酯。
化学名称为:9-[(R)-2-[[双[[(异丙氧基羰基)氧基]甲氧基] 氧膦基]甲氧基]丙基]腺嘌呤富马酸盐。
化学结构式: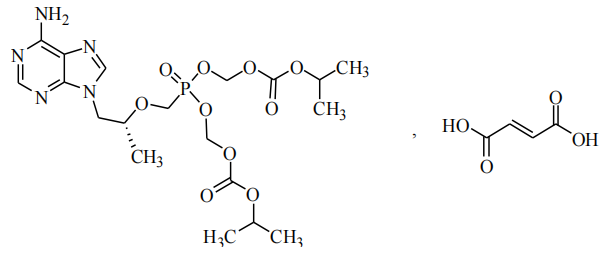
分子式:C19H30N5O10P·C4H4O4
分子量:635.51
本品内容物为白色或类白色粉末。
慢性乙型肝炎
富马酸替诺福韦二吡呋酯适用于治疗慢性乙肝成人和≥ 12岁的儿童患者。
在开始使用富马酸替诺福韦二吡呋酯治疗HBV感染时,应考虑到以下要点:
成人患者中该适应症的确立基于从初次接受核苷治疗的受试者和既往接受过治疗且证实拉米夫定耐药的受试者中获得的安全性和疗效数据。受试者为肝功能代偿的HBeAg阳性和HBeAg阴性慢性乙肝成人受试者。
富马酸替诺福韦二吡呋酯在数量有限的患有失代偿期肝病的慢性乙肝受试者中进行过评价。
临床试验中基线时存在阿德福韦相关突变的受试者数量太少,因此尚无法对疗效下结论。
成人和12岁及12岁以上儿童患者(35 kg或以上)推荐剂量
对慢性乙肝的治疗:剂量为每次300 mg(一粒),每日一次,口服,空腹或与食物同时服用。
对于慢性乙肝的治疗,最佳疗程尚未明确。体重小于35 kg的慢性乙肝儿童患者中的安全性和疗效尚未研究。
成人肾功能损害者使用剂量的调整
在中至重度肾功能损害的受试者中给予富马酸替诺福韦二吡呋酯时,药物暴露显著增加(参见【药代动力学”】。对基线肌酐清除率 <50 mL/分钟的患者,应按照表 1 调整富马酸替诺福韦二吡呋酯的给药间期。
在此推荐的给药间期是根据在不同肾功能损害级别的非 HIV 和非 HBV 感染受试者,包括需要血液透析的晚期肾病的患者中单次给药的药代动力学数据模型得出。
在中度到重度肾功能损害的患者中,尚未对这些给药间期调整建议的安全性和疗效进行临床评价,因此在这些患者中应当密切监测对治疗的临床反应和肾功能(参见【注意事项】)。
对轻度肾功能损害(肌酐清除率 50~80mL/分钟)的患者,无需调整剂量。在这些患者中应定期监测计算出来的肌酐清除率和血清磷。(参见【注意事项】)。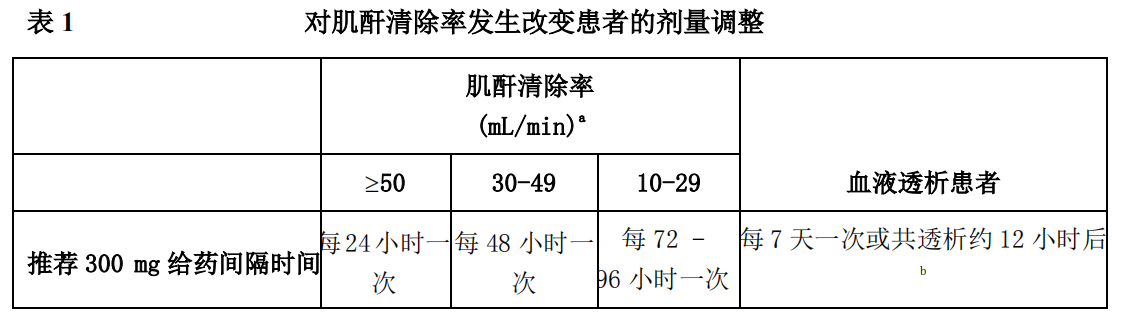
1. 使用理想(偏瘦)体重计算。
2. 一般每周一次(假定每周 3 次血液透析,每次大约持续 4 小时)。富马酸替诺福韦二吡呋酯应当在完成透析后给药。
在肌酐清除率<10mL/分钟的非血液透析患者中,尚未对替诺福韦的药代动力学进行评价,所以对这些患者没有给药建议。
尚无肾功能损害儿童患者给药建议数据。
使用富马酸替诺福韦二吡呋酯的患者,有罕见的肾功能损害、肾功能衰竭和近端肾小管病变(包括 Fanconi 综合征)的发生,并已有导致骨骼异常的报道(有时导致骨折)。推荐服用本品者进行肾功能监测。
富马酸替诺福韦二吡呋酯与其他抗逆转录病毒药物联用时,有接近三分之一的患者可能发生不良反应。这些不良反应通常是轻到中度的消化道事件。接近 1%服用富马酸替诺福韦二吡呋酯的成年患者因为消化道不良反应而中断治疗。
乳酸酸中毒、严重脂肪性肝肿大与富马酸替诺福韦二吡呋酯有关。
不推荐本品与去羟肌苷联用,因可导致不良反应风险的增加。有罕见的胰腺炎和乳酸酸中毒的报道,有时是致命的。
HBV 和 HIV 合并感染的患者在中断富马酸替诺福韦二吡呋酯治疗之后,曾有严重的乙型肝炎(HBV)急性恶化的报告。
以下不良反应基于文献(包括临床试验和上市后报告):
不良反应以器官系统、发生频率分类列于表 2。每一组的发生频率以降序排列,各发生频率定义如下:非常常见(≥1/10),常见(≥1/100,<1/10),不常见(≥1/100, <1/100),罕见(≥1/10000,<1/1000)。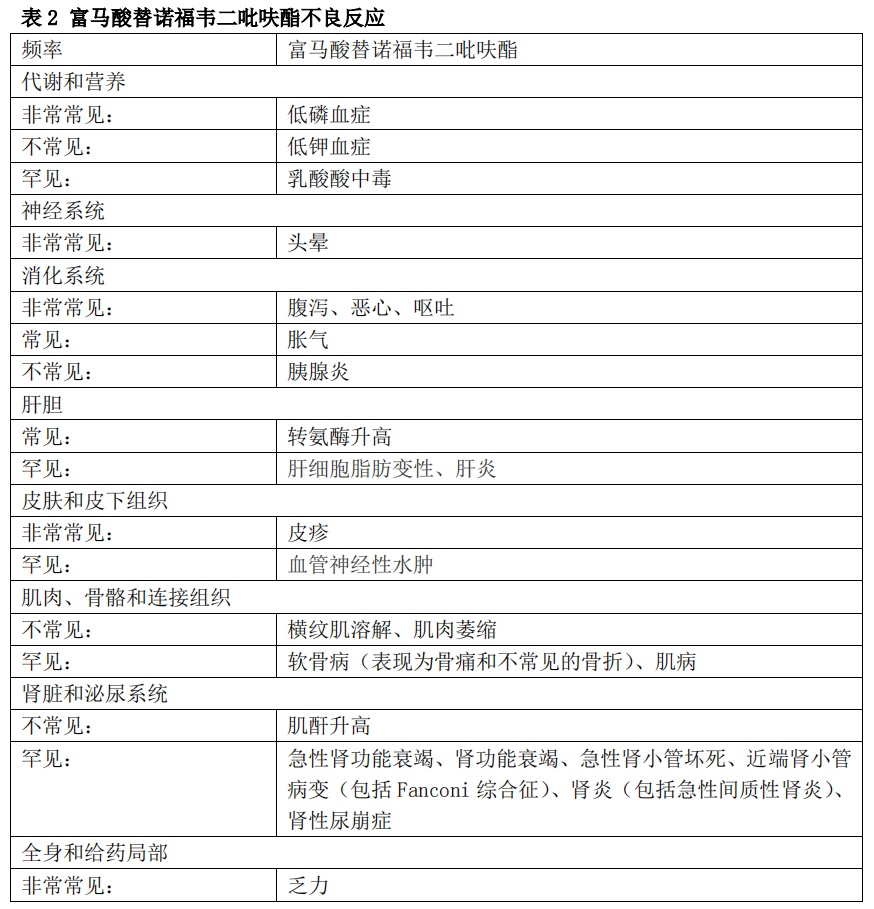
以下不良反应为临床使用过程中的自愿报告,其来源的人群大小未知,所以无法可靠估计其发生频率或建立其与药物暴露之间的因果关系。
免疫系统:过敏反应,包括神经性水肿;
代谢和营养:低磷血症、低钾血症、乳酸性酸中毒;
呼吸、胸和纵隔:呼吸困难;
胃肠道 :腹痛、淀粉酶增加和胰腺炎;
肝胆:脂肪肝、肝酶升高(最常见的天门冬氨酸转氨酶、丙氨酸转氨酶、丙种谷氨酰转肽酶)、肝炎;
皮肤和皮下组织:皮疹;
肌肉骨骼和结缔组织:横纹肌溶解症、骨软化症(表现为骨痛,可能造成骨折)、 肌无力、肌病(都与近端肾小管病变有关);
肾和泌尿系统:肾功能不全、肾衰、急性肾衰、Fanconi 综合征、近端肾小管病变、蛋白尿、肌酐升高、急性肾小管坏死、肾性尿崩症、多尿和间质性肾炎(包括急性病例);全身与用药部位:衰弱。
以下不良反应(已在上述身体系统标题下列出),可能由近端肾小管病变引起:横纹肌溶解症、骨软化症、低钾血症、肌无力、肌病、低磷血症 。
富马酸替诺福韦二吡呋酯禁用于先前对本药物中任何一种成份过敏的患者。
乳酸酸中毒/重度脂肪性肝肿大和中断治疗后肝炎恶化 核苷类似物(包括富马酸替诺福韦二吡呋酯片)与其它抗逆转录病毒药物联合用药治疗中,已经报告有乳酸酸中毒和重度脂肪性肝肿大,其中包括致死性病例(参见【注意事项】)。 在中止抗乙肝治疗(包括富马酸替诺福韦二吡呋酯片)的HBV感染患者中已有报告发生重度肝炎急性加重。对于中止抗乙肝治疗(包括富马酸替诺福韦二吡呋酯片)的患者,应在至少数月的临床和实验室随访中,对肝功能进行密切监测。必要时,可对患者重新进行抗乙肝治疗(参见【注意事项】)。
乳酸性酸中毒/严重脂肪性肝肿大
单独使用核苷类似物治疗或联用其它抗逆转录病毒药物治疗时,曾有发生乳酸性酸中毒和严重脂肪性肝肿大的报告,包括出现致死病例。这些病例大多数发生在女性中。 肥胖及对核苷的长期暴露 可能是危险因素。在有已知肝病危险因素的患者中给予核苷类似物时要特别注意;然而,在没有已知危险因素的患者中也曾经有病例报告。 任何患者的临床或实验室结果如果提示有乳酸性酸中毒或显著的肝毒性(可能包括肝肿大和脂肪变性,即便转氨酶没有显著升高),应当暂停富马酸替诺福韦二吡呋酯治疗。
中断治疗后乙肝恶化
对感染 HBV 但中断富马酸替诺福韦二吡呋酯治疗的患者必须严密监测,包括临床及实验室随访在停止治疗后还要持续至少几个月的时间。如果条件适当,可以准许患者重新开始抗乙肝病毒治疗。
新出现的或更严重的肾功能损害
替诺福韦主要通过肾脏清除。 使用富马酸替诺福韦二吡呋酯时,曾有其引起肾功能损害的报告,包括出现急性肾衰和 Fanconi 综合征(肾小管损伤伴严重低磷酸血症)的病例。
建议在开始治疗前以及使用富马酸替诺福韦二吡呋酯治疗期间临床上适当时对所有患者进行肌酐清除率计算。 对有肾功能损害风险的患者,包括先前在接受阿德福韦酯治疗时经历过肾脏不良事件的患者,应定期监测计算出的肌酐清除率和血清磷。
建议对所有肌酐清除率低于 50 mL/分钟的患者调整富马酸替诺福韦二吡呋酯的给药间期,并密切监测其肾功能。在按照剂量调整指导接受富马酸替诺福韦二吡呋酯治疗的肾功能损害患者中,目前还没有可用的安全性或疗效数据,所以应当对接受富马酸替诺福韦二吡呋酯治疗的潜在受益和肾毒性的潜在风险进行评估。
如果目前或近期曾使用过有肾毒性的制剂,应当避免使用富马酸替诺福韦二吡呋酯治疗。
与其他药物联用
富马酸替诺福韦二吡呋酯不应与含有替诺福韦的固定剂量复方制剂联用,包括:依非韦伦/恩曲他滨/富马酸替诺福韦二吡呋酯,利匹韦林/恩曲他滨/富马酸替诺福韦二吡呋酯,艾维雷韦/克比司特/恩曲他滨/富马酸替诺福韦二吡呋酯,或恩曲他滨替诺福韦。
HIV-1 和 HBV 合并感染的患者
因存在 HIV-1 耐药风险,富马酸替诺福韦二吡呋酯仅可作为抗逆转录病毒联合治疗方案的一部分用于 HBV 和 HIV-1 合并感染患者。
所有 HBV 感染患者开始富马酸替诺福韦二吡呋酯治疗前应进行 HIV-1 抗体检查。也建议所有 HIV-1 感染患者开始富马酸替诺福韦二吡呋酯治疗前进行慢性乙肝的检查。
药物相互作用
与富马酸替诺福韦二吡呋酯联合给药时,去羟肌酐缓释片或肠溶制剂的最大血清浓度(Cmax) 和血浆浓度时间曲线下面积(AUC) 显著升高(参见表)。 这种相互作用的机制尚未明确。 较高的去羟肌酐浓度有可能导致与去羟肌酐有关的不良事件,包括胰腺炎和外周神经病变。
在接受替诺福韦和去羟肌酐每天 400 mg 的患者中,观察到 CD4+ 细胞计数下降。
在体重>60 kg 的患者中,与富马酸替诺福韦二吡呋酯联用时,去羟肌酐的剂量应当减至 250 mg。 在体重<60 kg 的成人或儿童患者中,目前还没有去羟肌酐剂量调整建议的数据。联合给药时,富马酸替诺福韦二吡呋酯和去羟肌酐肠溶剂可以在空腹状态下或与清淡食物(<400 Kcal,20% 脂肪)同时给药。 去羟肌酐缓释片与富马酸替诺福韦二吡呋酯应当在空腹状态下联合给药。
富马酸替诺福韦二吡呋酯与去羟肌酐联合给药时应当谨慎,接受联合用药的患者应当密切监测与去羟肌酐有关的不良事件。在出现与去羟肌酐相关的不良反应的患者中,应当停用去羟肌酐。
因为替诺福韦主要通过肾脏清除,所以富马酸替诺福韦二吡呋酯与能够导致肾功能减低或与肾小管主动清除竞争的药物合用,能够使替诺福韦的血清浓度升高和/或使其他经肾脏清除的药物浓度增高。此类药物包括但不限于阿德福韦酯、西多福韦、阿昔洛韦、万乃洛韦、更昔洛韦和缬更昔洛韦。
较高的替诺福韦浓度有可能导致富马酸替诺福韦二吡呋酯相关的不良事件,包括肾脏疾病。
阿扎那韦 和洛匹那韦/利托那韦可使替诺福韦浓度增加。 这种相互作用的机制尚未明确。 在接受洛匹那韦/利托那韦和富马酸替诺福韦二吡呋酯的患者中,应当监测其与富马酸替诺福韦二吡呋酯相关的不良反应。 在出现与富马酸替诺福韦二吡呋酯相关的不良事件的患者中,应当停用富马酸替诺福韦二吡呋酯。
富马酸替诺福韦二吡呋酯能够降低阿扎那韦的 AUC 和 Cmin 。与富马酸替诺福韦二吡呋酯合用时,建议阿扎那韦 300 mg 与利托那韦 100 mg 同时给药。如果没有利托那韦,阿扎那韦不应与与富马酸替诺福韦二吡呋酯联合给药。
骨效应 在临床研究中发现,接受过富马酸替诺福韦二吡呋酯治疗的 HIV 感染成人患者中,腰椎和髋部的骨矿物质密度(BMD)相对于基线下降。骨矿物质密度的下降大部分发生在试验的前 24~48 周,直至第 144 周,下降保持稳定。并有患者报告了临床上相关的骨折(手指和脚趾除外)。 此外,富马酸替诺福韦二吡呋酯组中骨代谢的生化标记物(血清骨特异性碱性磷酸酶、血清降钙素、血清羧基端肽、尿氨基端肽)显著升高,提示骨转化增加。 富马酸替诺福韦二吡呋酯组中血清甲状旁腺激素水平和 1,25 维生素 D 水平也较高。富马酸替诺福韦二吡呋酯相关的骨矿物质密度和生化标记物变化对长期骨健康和未来骨折风险的影响仍然未明确。
曾经报道过与使用富马酸替诺福韦二吡呋酯有关的骨软化症(与近端肾小管病变有关)病例。(参见【不良反应】)
在有病理性骨折或有骨硬化症或有骨流失风险的 HIV 感染患者中,应当考虑骨监测。
尽管没有对补充钙和维生素 D 的作用进行研究,但这样的补充可能对所有患者都有益。 如果怀疑有骨异常,应进行适当的会诊。
脂肪重新分布
接受抗反转录病毒联合治疗的 HIV 感染患者中,曾经观察到体脂重新分布/堆积包括向心性肥胖、项背脂肪增加(水牛背)、周围消瘦、面部消瘦、胸部增大和柯兴氏样面容。这些现象发生的机制和长期后果目前未明确。 因果关系尚未确立。
免疫重建炎性综合征
接受包括富马酸替诺福韦二吡呋酯在内抗反转录病毒联合治疗的 HIV 感染患者中,曾经报告过免疫重建炎性综合征。在抗反转录病毒联合治疗的初期,患者的免疫应答系统有可能对顽固性或残余的机会性感染产生炎症反应(例如鸟结核分枝杆菌感染、巨细胞病毒、耶氏肺孢子菌肺炎(PCP),或结核),对此有必要更进一步评价和治疗。
此外,曾有在免疫重建治疗时发生自身免疫失调(例如格雷夫斯病、多发性肌炎和格林-巴利综合征)的报告,然而,发病的时间更多样化,也可能在开始治疗后数个月内发生。
早期病毒学失败
HIV 感染受试者中的临床试验证明,与包含两种核苷反转录酶抑制剂和一种非核苷反转录酶抑制剂或一种 HIV 蛋白酶抑制剂的三联药物治疗方案相比,某些只包含三种核苷类反转录酶抑制剂(NRTI)的药物治疗方案总体上有效性较弱。 尤其应考虑到已有早期病毒学失败和高耐药性替代的报告。 因而应谨慎使用三联核苷治疗方案。 对使用三联核苷类方案治疗的患者,应仔细监测并考虑改进疗法。
在高于 富马酸替诺福韦二吡呋酯 300 mg 治疗剂量下的临床经验很有限。 临床研究中,曾有 8 名患者接受了持续 28 天的口服富马酸替诺福韦二吡呋酯 600 mg 治疗。 没有发生严重不良反应的报告。 更高剂量可能产生的影响尚不清楚。
如果发生服用过量,必须监测患者是否有中毒的证据,如有必要,应采用标准的支持性治疗方案。
替诺福韦能够被血液透析有效清除,萃取系数大约为 54%。 富马酸替诺福韦二吡呋酯300 mg 单次给药后,一次 4 小时的血液透析大约能清除替诺福韦给药剂量的 10% 。
美国妊娠分级 B 类: 在大鼠和家兔中进行了生殖研究,根据体表面积比较的剂量最高分别为人的 14 和 19倍,结果显示没有证据表明因为替诺福韦造成生育力受损害或对胚胎有伤害。 然而,没有在妊娠妇女中进行过充分及有良好对照的研究。 由于动物生殖研究并不是总能预测人的反应,因此在妊娠期内不应使用富马酸替诺福韦二吡呋酯,除非十分需要。美国疾病控制和预防中心建议,HIV 感染的妇女不应以母乳喂养她们的婴儿,以避免出生后 HIV 传播的风险。 在大鼠中进行的研究证明替诺福韦被分泌到乳汁中。 在人类中,取自产后一周内的五名 HIV-1 感染妇女的乳液样本显示,有少量替诺福韦被分泌到人乳中。 这种暴露对哺乳期婴儿的影响尚未明确。 因为 HIV 传播和严重的不良反应都有可能在哺乳婴儿中发生,所以母亲如果正在接受富马酸替诺福韦二吡呋酯治疗,应当要求她们不要以母乳喂养。已有国外临床研究数据支持富马酸替诺福韦二吡呋酯用于治疗2至18岁的HIV-1患者的安全性。并有研究数据表明,富马酸替诺福韦二吡呋酯在推荐的剂量范围内,在2~18岁患者的体内药代特征与临床试验中建立的成人安全有效剂量的药代特征是相似的。 用于 2 岁以下儿童的安全性和有效性尚未建立。富马酸替诺福韦二吡呋酯的临床研究没有入选足够数量的年满 65 岁或以上的受试者,无法判定他们的应答是否与较年轻的受试者的应答不同。 一般而言,老年患者心、肝、肾功能下降,并发疾病或正在使用其他药物的几率增加,选择剂量应谨慎。
B级:
在明显高于(~300 倍)体内所观察到的浓度时,替诺福韦在体外没有对下列任意一种人 CYP450 异构体介导的体外药物代谢产生抑制作用。 CYP3A4、CYP2D6、CYP2C9 或CYP2E1。 然而,在 CYP1A 底物的代谢中观察到小幅度(6%)但具有统计学意义的降低。 根据体外实验结果和已知的替诺福韦清除途径,替诺福韦与其他药品之间存在由 CYP450 介导的相互作用的可能性很小。 (参见【药代动力学】)。
替诺福韦主要通过肾小球过滤和肾小管主动清除结合的方式被清除。 富马酸替诺福韦二吡呋酯与能够导致肾功能减低或与肾小管主动清除竞争的药物联合用药,能够使替诺福韦的血清浓度升高和/或使其他经肾脏清除的药物浓度增高。能够降低肾功能的药物也有可能增加替诺福韦的血清浓度。
在健康志愿者中,通过与阿扎那韦、去羟肌酐、依非韦伦、恩曲他滨、茚地那韦、拉米夫定、洛匹那韦/利托那韦、美沙酮、奈非那韦、口服避孕药、利巴韦林、沙奎那韦/利托那韦和他克莫司联合用药,对富马酸替诺福韦二吡呋酯进行了评价。 表 3 和表 4 总结了合用药物对替诺福韦药代动力学的影响以及富马酸替诺福韦二吡呋酯对合用药物药代动力学的影响。
表5总结了富马酸替诺福韦二吡呋酯和去羟肌酐之间的药物相互作用。 富马酸替诺福韦二吡呋酯与去羟肌酐联合给药时应当谨慎。当与富马酸替诺福韦二吡呋酯多次给药联合用药时,去羟肌酐 400 mg 的 Cmax 和 AUC 显著增高。 这种相互作用的机制尚未明确。去羟肌酐 250 mg 的肠溶胶囊与富马酸替诺福韦二吡呋酯联合用药时,对去羟肌酐的全身暴露水平与空腹状态下 400 mg 肠溶胶囊单独使用时相似。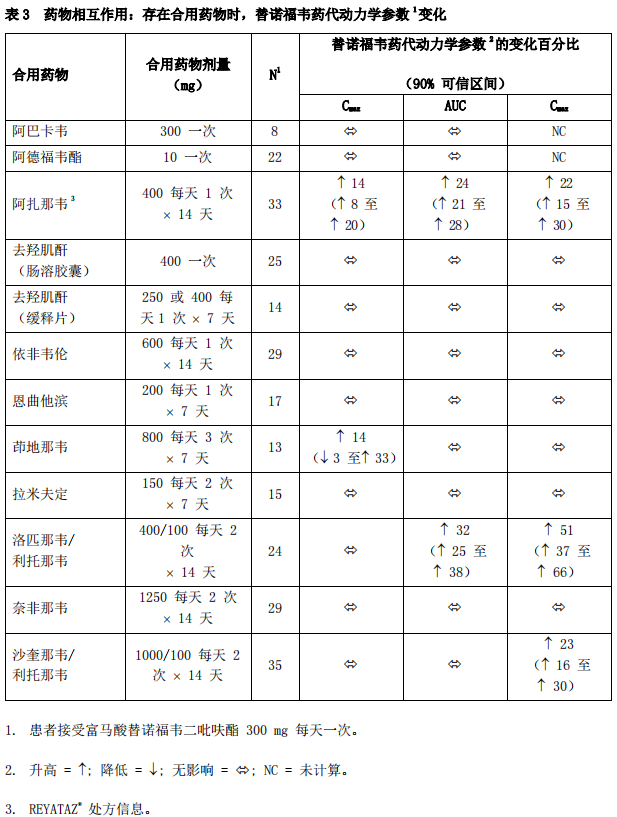
接受长期美沙酮维持治疗或口服避孕药或单次利巴韦林治疗的 HIV 阴性受试者,多次给予富马酸替诺福韦二吡呋酯后,稳定状态下替诺福韦的药代动力学和先前研究中所观察到的相似,表明这些药物和富马酸替诺福韦二吡呋酯之间不存在有临床意义的药物相互作用。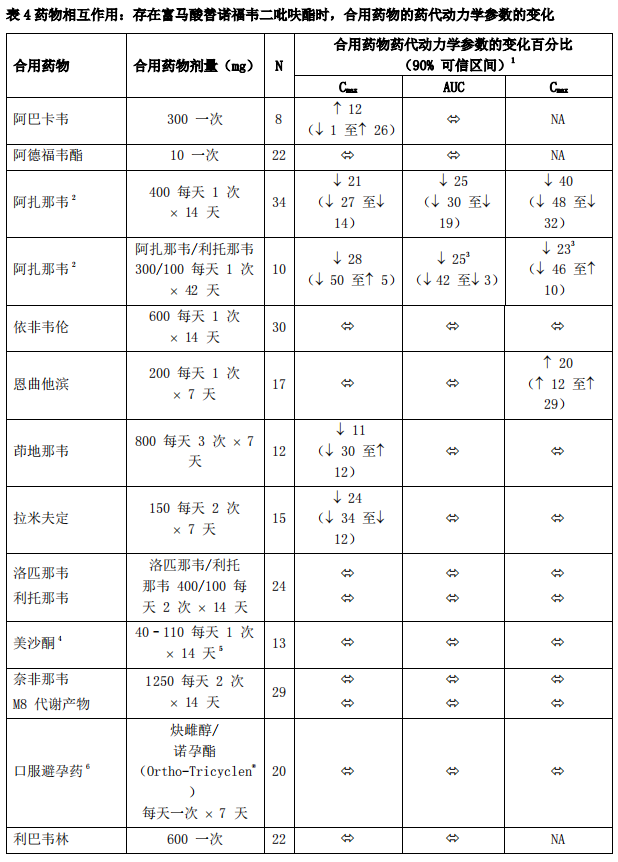
福建广生堂药业股份有限公司
86904771000460
作用机制:富马酸替诺福韦酯是一种一磷酸腺苷的开环核苷膦化二酯结构类似物。富马酸替诺福韦二吡呋酯首先需要经二酯的水解转化为替诺福韦,然后通过细胞酶的磷酸化形成二磷酸替诺福韦,也叫链末端终止剂。二磷酸替诺福韦通过与天然底物 5'-三磷酸脱氧腺苷竞争,并且在与 DNA 整合后终止 DNA 链,从而抑制 HIV-1 反转录酶和 HBV 反转录酶的活性。二磷酸替诺福韦对哺乳动物 DNA 聚合酶α、β和线粒体 DNA 聚合酶γ是弱抑制剂。
抗 HIV 活性:
抗病毒活性:在淋巴母细胞系、原代单核细胞/巨噬细胞和外周血淋巴细胞中评估了替诺福韦抗实验室和临床分离 HIV-1 抗病毒活性。替诺福韦的 EC50(50%有效浓度)值在0.04 μM 至 8.5μM 之间。在替诺福韦与核苷反转录酶抑制剂(阿巴卡韦、去羟肌苷、拉米夫定、司他夫定、扎西他滨、齐多夫定)、非核苷反转录酶抑制剂(地拉韦定、依非韦伦、奈韦拉平)、蛋白酶抑制剂(安普那韦、茚地那韦、奈非那韦、利托那韦、沙奎那韦)联合用药的研究中,替诺福韦没有拮抗作用。在细胞培养中替诺福韦对 HIV-1 的亚型 A、B、C、D、 E、F、G、O 有抗病毒活性(EC50值范围为:0.5μM 至 2.2μM),对 HIV-2 有因病毒株而异的活性(EC50值范围为:1.6 μM 至 5.5μM)。
耐药性:在细胞培养中挑选出了对替诺福韦敏感性降低的 HIV-1 分离病毒株。 这些病毒的反转录酶都出现 K65R 突变,对替诺福韦的敏感性降低了 2–4 倍。
在对未接受过治疗的受试者进行的临床研究中(富马酸替诺福韦二吡呋酯+拉米夫定+依非韦伦与司他夫定+拉米夫定+依非韦伦),对 144 周内病毒学失败受试者中分离的病毒株进行了基因分析,结果显示与依非韦伦和拉米夫定耐药有关的突变最为常见,两个治疗组之间没有差异。在所分析的患者分离病毒株中,富马酸替诺福韦二吡呋酯组中 K65R 突变的发生率为 8/47(17%),司他夫定组为 2/49(4%)。富马酸替诺福韦二吡呋酯组 144 周内病毒出现 K65R 的 8 名受试者中,有 7 名发生在治疗的前 48 周内,另 1 名发生在第 96 周。该研究中没有发现其他导致对富马酸替诺福韦二吡呋酯耐药的突变。
在对未经治疗的受试者进行的临床研究中(富马酸替诺福韦二吡呋酯+恩曲他滨+依非韦伦与齐多夫定/拉米夫定+依非韦伦),对所有在第 144 周 HIV-1 RNA >400 拷贝/mL 确认病毒学应答失败的或提前终止治疗的受试者中分离出的 HIV-1 进行了基因型分析。结果显示出现依非韦伦耐药相关的突变最为常见,两个治疗组中相似。在所分析的受试者分离病毒株中,与恩曲他滨和拉米夫定耐药有关的 M184V 突变在富马酸替诺福韦二吡呋酯+恩曲他滨组发生频率为 2/19,在齐多夫定/拉米夫定组为 10/29。 在持续 144 周的研究 934 中,使用标准的基因型分析,没有在受试者的 HIV-1 中检测到 K65R 突变。
交叉耐药性:某些特定反转录酶抑制剂之间存在着交叉耐药性。由替诺福韦筛选出的K65R 突变在一些接受阿巴卡韦、去羟肌苷、或扎西他滨治疗的 HIV-1 感染受试者中也被筛选出来。含有这种突变的 HIV 分离病毒株对恩曲他滨和拉米夫定的敏感性下降。因此,在携有 K65R 突变的患者中可能发生对这些药物的交叉耐药。从 20 名平均出现 3 种与齐多夫定相关的反转录酶突变(M41L、D67N、K70R、L210W、T215Y/F、K219Q/E/N)的受试者中分离出的 HIV-1 病毒株显示,对替诺福韦的敏感性下降了 3.1 倍。
在对接受过治疗的受试者进行的临床研究中(富马酸替诺福韦二吡呋酯+标准背景治疗(SBT)与安慰剂+标准背景治疗),第 96 周期间接受富马酸替诺福韦二吡呋酯治疗发生病毒学失败的受试者有 14/304(5%),对替诺福韦的敏感性下降超过 1.4 倍(中位值为 2.7 倍)。对在基线和失败时分离出的病毒株进行基因型分析的结果表明,HIV-1 反转录酶基因中出现了 K65R 突变。
在参加临床研究接受过治疗的受试者中,在基线病毒基因型(N=222)方面评价了患者对富马酸替诺福韦二吡呋酯的病毒学反应。
在这些临床试验中,94% 接受评价参与者的基线 HIV-1 分离病毒株表达了至少一种核苷反转录酶抑制剂(NRTI)突变。在基因亚型研究中,受试者病毒学反应与总体试验结果相似。
几项探索性分析评价了特定突变和突变模式对病毒学结果的影响。因为存在大量的比较方式,所以没有进行统计学检验。富马酸替诺福韦二吡呋酯对先前存在的与齐多夫定耐药相关的突变(M41L、D67N、K70R、L210W、T215Y/F、或 K219Q/E/N)呈现不同程度交叉耐药性,其程度与特定突变的数目与种类相关。接受富马酸替诺福韦二吡呋酯治疗、出现 3种或以上齐多夫定耐药相关突变(包含了 M41L 或 L210W 反转录酶突变)的 HIV-1 受试者对富马酸替诺福韦二吡呋酯治疗的应答降低;然而与安慰剂相比,这些受试者应答仍显示改善。D67N、K70R、T215Y/F、K219Q/E/N 突变的出现,似乎不影响对富马酸替诺福韦二吡呋酯治疗的应答。病毒出现 L74V 取代基因突变但无齐多夫定耐药相关取代基因突变的受试者(N=8)对富马酸替诺福韦二吡呋酯应答下降。病毒表达 Y115F(N=3)、Q151M(N=2)取代基因突变或 T69 插入基因突变(N=4)的受试者相关数据有限,所有受试者应答均下降。在试验方案规定的分析中,出现与阿巴卡韦/恩曲他滨/拉米夫定耐药相关的 M184V 突变的 HIV-1 受试者对富马酸替诺福韦二吡呋酯的病毒学应答没有降低。这些患者中 HIV-1 RNA 反应在第 48 周期间持续存在。
研究 902 和 907 表型分析:接受过治疗的受试者(N=100)基线 HIV-1 表型分析表明,基线病毒对富马酸替诺福韦二吡呋酯的敏感性和患者对富马酸替诺福韦二吡呋酯治疗的应答之间存在相关性。表 8 按照基线富马酸替诺福韦二吡呋酯的敏感性总结了 HIV-1 RNA 的应答。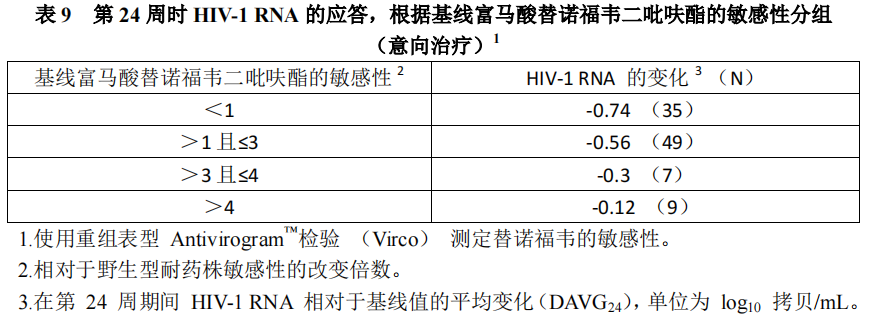
抗 HBV 活性
抗病毒活性:在 HepG2 2.2.15 细胞系中对替诺福韦抗 HBV 的抗病毒活性进行评估,替诺福韦的 EC50值在 0.14~1.5 μM 之间,CC50(50%细胞毒性浓度)值大于 100 μM。在细胞培养中研究替诺福韦与核苷类 HBV 逆转录酶抑制剂恩替卡韦、拉米夫定和替比夫定,以及与核苷类 HIV-1 逆转录酶抑制剂恩曲他滨联合用药的抗病毒活性,未观察到任何拮抗作用。
耐药性:对于研究 0102、0103、0106、0108、0121 和 LOC114648 中接受富马酸替诺福韦二吡呋酯单药治疗至少 24 周但在每研究年末时(或终止富马酸替诺福韦二吡呋酯单药治疗时)病毒血症 HBV DNA 仍大于或等于 400 拷贝/毫升的受试者,用其治疗前和治疗期间配对的分离 HBV 逆转录酶氨基酸序列(部分或全段序列)样本进行每年一次至 240 周的富马酸替诺福韦二吡呋酯累积基因型耐药评估。研究 0102 和 0103 核苷初治人群中,HBeAg阳性受试者基线病毒载量高于 HBeAg 阴性受试者,并且在富马酸替诺福韦二吡呋酯单药治疗末次给药时间点时仍呈现病毒血症受试者比率显著较高(分别为 15%和 4%)。
仍呈现病毒血症受试者的 HBV 分离株显示有治疗期间出现的突变(表 10);但是,并未出现发生率高且与富马酸替诺福韦二吡呋酯耐药(基因型和表型分析)相关的特定突变。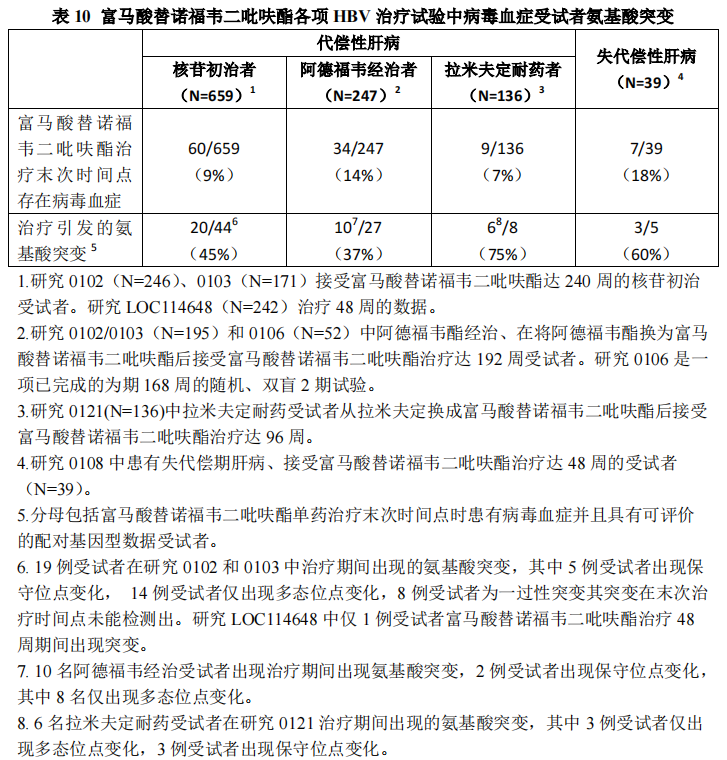
交叉耐药:在 HBV 核苷/核苷酸类似物逆转录酶抑制剂之间观察到交叉耐药。
基于细胞试验,拉米夫定和替比夫定耐药相关 rtV173L、rtL180M 和 rtM204I/V 突变的HBV 病毒株对替诺福韦的敏感性为野生型病毒的 0.7 至 3.4 倍。rtL180M 和 rtM204I/V 双突变后对替诺福韦的敏感性降低 3.4 倍。
恩替卡韦耐药相关 rtL180M、rtT184G、rtS202G/I、rtM204V 和 rtM250V 突变的 HBV病毒株对替诺福韦的敏感性为野生型病毒的 0.6 至 6.9 倍。
阿德福韦耐药相关 rtA181V 和/或 rtN236T 突变的 HBV 病毒株对替诺福韦的敏感性为野生型病毒的 2.9 至 10 倍,携带 rtA181T 突变基因的病毒株对替诺福韦的敏感性为野生型病毒的 0.9 至 1.5 倍。
研究 0102、0103、0106、0108 和 0121 中有 152 名受试者在开始接受富马酸替诺福韦二吡呋酯治疗时 HBV 携带已知对 HBV 核苷/核苷酸类似物逆转录酶抑制剂耐药的突变基因:14 名携带阿德福韦耐药相关突变基因(rtA181S/T/V 和/或 rtN236T),135 名携带拉米夫定耐药相关突变基因(rtM204I/V),3 名携带阿德福韦和拉米夫定耐药相关突变基因。在使用富马酸替诺福韦二吡呋酯治疗长达 240 周后,11/14 名阿德福韦耐药 HBV 受试者、124/135 名拉米夫定耐药 HBV 受试者和 2/3 名阿德福韦和拉米夫定耐药 HBV受试者均达到并维持病毒抑制(HBV DNA 小于 400 拷贝数/mL)。3/5 名携带 rtA181T/V 和 rtN236T 突变病毒的受试者仍有病毒血症。
遗传毒性
富马酸替诺福韦二吡呋酯在体外小鼠淋巴试验中能导致基因突变,在 Ames 试验中结果为阴性。在一项体内小鼠微核试验中,富马酸替诺福韦二吡呋酯对雄性小鼠给药结果为阴性。
生殖毒性
根据体表面积比较,在大鼠中以相当于人 10 倍的剂量给予富马酸替诺福韦二吡呋酯,雄性大鼠在交配前连续 28天给予药物、雌性大鼠在交配前到妊娠第 7 天连续 15天给予药物,结果显示富马酸替诺福韦二吡呋酯对生育能力、交配行为和早期胚胎发育均未见影响。然而,在雌性大鼠中出现发情周期的改变。
致癌性
在小鼠和大鼠中进行了富马酸替诺福韦二吡呋酯的长期经口给药致癌性研究,暴露水平最高大约分别为人体 HIV-1 感染治疗剂量的 16 倍(小鼠)和 5 倍(大鼠)。 雌性小鼠在高剂量下(暴露水平比人高 16 倍)肝脏腺瘤增加。大鼠最高暴露水平是人治疗剂量 5 倍时,未见致癌性。
其它毒性
在毒理学研究中,以大于或等于 6 倍的人体暴露水平(以 AUC 计)对大鼠、犬、猴给予替诺福韦和富马酸替诺福韦二吡呋酯,出现了骨毒性。在猴中,骨毒性被诊断为骨软化症。在猴中,替诺福韦减量或停用后,骨软化症呈现出可逆性。在大鼠和犬中,骨毒性表现为骨矿物质密度降低。骨毒性的潜在机制未知。
在 4 种动物中发现了肾毒性的证据。在这些动物中,观察到了不同程度的血清肌酐、尿酸氮、糖尿、蛋白尿、磷酸尿、和/或钙尿增加以及血磷降低。这些毒性是在比人高 2~20倍的暴露水平(以 AUC 计)下观察到的。肾脏异常尤其是磷酸尿与骨毒性的关系未知。
在健康志愿者和 HIV-1 感染者中评价了富马酸替诺福韦二吡呋酯的药代动力学。 这些人群中替诺福韦的药代动力学相似。
吸收:富马酸替诺福韦二吡呋酯是活性成分替诺福韦的水溶性双酯前体药物。在空腹服用富马酸替诺福韦二吡呋酯的患者中,替诺福韦的口服生物利用度大约为 25%。 在空腹状态下,HIV-1 感染患者单次口服富马酸替诺福韦二吡呋酯 300mg,在 1.0±0.4 小时内达到最高血清浓度(Cmax)。Cmax 和 AUC 值分别是 296± 90ng/mL 和 2287±685ng·小时/mL。
在富马酸替诺福韦二吡呋酯剂量为 75–600mg 之间时,替诺福韦的药代动力学和剂量呈比例关系,不受重复给药的影响。
食物对口服吸收的影响:在进食高脂肪餐(~700–1000 kcal,含 40%–50% 的脂肪)后,口服富马酸替诺福韦二吡呋酯 300 mg,口服生物利用度增加, 替诺福韦 AUC0-∞增加约40%,Cmax增加约 14%。 然而富马酸替诺福韦二吡呋酯和清淡食物一起给药时,与空腹给药相比,对替诺福韦的药代动力学没有显著影响。 食物使替诺福韦到达 Cmax 的时间延迟了大约 1 小时。 在进食状态下,不控制食物的成分,富马酸替诺福韦二吡呋酯 300 mg 每天一次,多次给药后替诺福韦的 Cmax 和 AUC 分别是 0.33 ± 0.12μg/mL 和 3.32 ±1.37μg•hr/mL。
分布:在替诺福韦浓度范围 0.01~25 μg/mL 之间,其在体外与人血浆或血清蛋白的体内结合率分别小于 0.7% 和 7.2%。替诺福韦以 1.0mg/kg 和 3.0mg/kg 的剂量静脉注射给药后,稳态分布容积分别是 1.3 ±0.6L/kg 和 1.2±0.4L/kg。
代谢和清除:体外研究表明,替诺福韦二吡呋酯和替诺福韦都不是 CYP450 酶的底物。
替诺福韦静脉注射给药后 72 小时内,在尿液中以替诺福韦药物原型的形式大约回收了给药剂量的 70%–80%。 富马酸替诺福韦二吡呋酯单次口服给药后,替诺福韦的终末半衰期大约为 17 小时。 富马酸替诺福韦二吡呋酯 300mg 每天一次多次口服给药后(进食状态下),24 小时内在尿液中可回收给药剂量的 32±10%。
替诺福韦通过肾小球过滤和肾小管主动清除结合的方式被清除。与其他通过肾脏被清除的药物可能产生清除方面的竞争。
特殊人群
种族:目前除了白种人以外,没有足够的种族和民族数据能够充分判断这些人群之间可能存在的药代动力学差异。
性别:在男性和女性患者中,替诺福韦的药代动力学相似。
儿童:52 例 HBV 感染儿童受试者(12 至< 18 岁)口服富马酸替诺福韦二吡呋酯 300 mg片每日一次后,替诺福韦的暴露量与 HIV-1 感染成人及儿童暴露量相似。
老年人:在老年人(>65 岁)中没有进行药代动力学研究。
肝功能损害:在中度到重度肝功能损害的非 HIV 感染患者中,富马酸替诺福韦二吡呋酯 300 mg 单次给药后,对替诺福韦的药代动力学进行了研究。 与没有肝功能损害的患者相比,肝功能损害的患者中替诺福韦的药代动力学没有实质性的改变。 在肝功能损害的患者中不需要改变富马酸替诺福韦二吡呋酯的给药剂量。
肾功能损害:肾功能损害的患者中替诺福韦的药代动力学发生改变。在肌酐清除率低于 50mL/分钟或晚期肾病(ESRD)要求透析的患者中,替诺福韦的 Cmax 和 AUC0-∞增加表 7。
建议在肌酐清除率 <50 mL/分钟的患者中或在患晚期肾病要求透析的患者中更改富马酸替诺福韦二吡呋酯的给药间期(参见【用法用量】)。
表 7 在肾功能级别不同的患者中替诺福韦*的药代动力学参数(均值±标准差)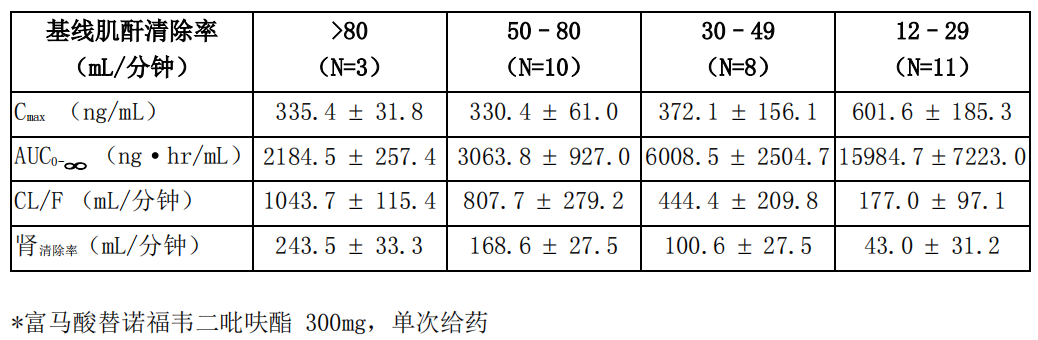
替诺福韦能够被血液透析有效清除,萃取系数大约为 54%。富马酸替诺福韦二吡呋酯300 mg 单次给药后,一次 4 小时的血液透析大约能清除替诺福韦给药剂量的 10% 。
胶囊剂
300mg
铝塑包装,每板 7 粒,每盒 1 板;药用塑料瓶,14 粒/瓶。
遮光、密封,在阴凉干燥处保存。
24 个月
国药准字H20170005

