全欣达(Kesimpta)说明书
Ofatumumab Injection
奥法妥木单抗
活性成份:
奥法妥木单抗是一种重组人单克隆免疫球蛋白 G1(IgG1)抗体,可与 B 细胞上表达的人 CD20 结合。奥法妥木单抗由鼠 NS0 细胞系生产。
辅料:L-精氨酸、依地酸二钠、聚山梨酯 80、醋酸钠三水合物、氯化钠、注射用水和 25%盐酸。
本品为澄清至略带乳光、无色至微棕黄色溶液。
奥法妥木单抗适用于治疗成人复发型多发性硬化(RMS),包括临床孤立综合征、复发缓解型多发性硬化和活动性继发进展型多发性硬化。
在首次使用奥法妥木单抗之前进行评估乙肝病毒筛查
在开始奥法妥木单抗治疗前,进行乙肝病毒(HBV)筛查。奥法妥木单抗禁用于乙肝表面抗原 [HBsAg]和抗 HBV 阳性检测结果证实的活动性 HBV 患者。对于 HBsAg 阴性且乙肝核心抗体阳性 [HBcAb +] ,或 [HBsAg +] 的 HBV 携带者,在开始奥法妥木单抗治疗前和治疗期间请咨询肝病专家(参见【注意事项】)。
血清免疫球蛋白
开始奥法妥木单抗治疗前,进行定量血清免疫球蛋白检测(参见【注意事项】)。对于血清免疫球蛋白水平较低的患者,在开始奥法妥木单抗治疗前请咨询免疫学专家。
疫苗接种
由于不建议在治疗期间和停药后直至B 细胞水平恢复正常之前接种减毒活疫苗或活疫苗,因此根据免疫接种指南,在开始奥法妥木单抗治疗前至少 4 周接种活疫苗或减毒活疫
苗,以及在可能的情况下,在开始奥法妥木单抗治疗前至少 2 周接种灭活疫苗(参见【注意事项】)。
推荐剂量
奥法妥木单抗的推荐剂量为:
在第 0、1 和 2 周,皮下注射初始剂量 20 mg,
从第 4 周开始,每月一次皮下注射 20 mg。漏给药
如果漏注射了奥法妥木单抗,应尽快给药,而不必等到下一个预定的给药时间。随后应按建议的间隔时间给药。
用药说明
仅可通过皮下注射给药。
奥法妥木单抗适用于患者自行皮下注射给药。
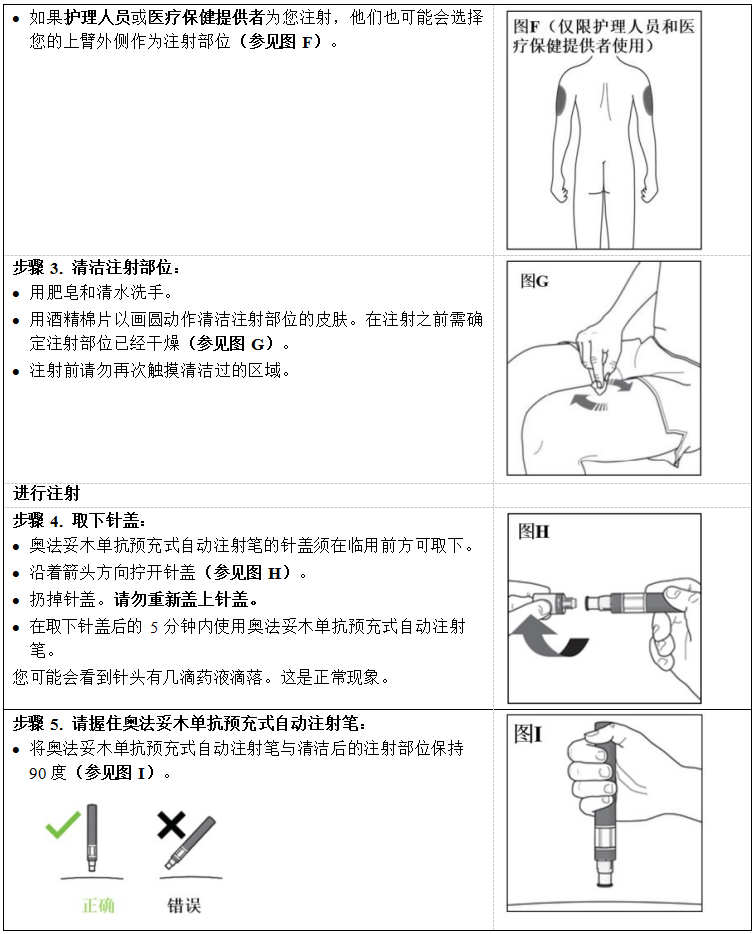
在腹部、大腿或上臂外侧通过皮下注射奥法妥木单抗。请勿注射到痣、瘢痕、伸展纹或存在皮肤压痛、瘀伤、发红、有鳞屑或有硬块的区域。
第一次注射奥法妥木单抗应在接受过相应培训的医疗保健专业人士的指导下进行(参见【注意事项】)。
奥法妥木单抗预充式自动注射笔仅供一次性使用,使用后应丢弃。有关完整的用药说明,参见使用说明。
奥法妥木单抗的制备
有关奥法妥木单抗制备的更详细的说明,参见奥法妥木单抗的使用说明书。
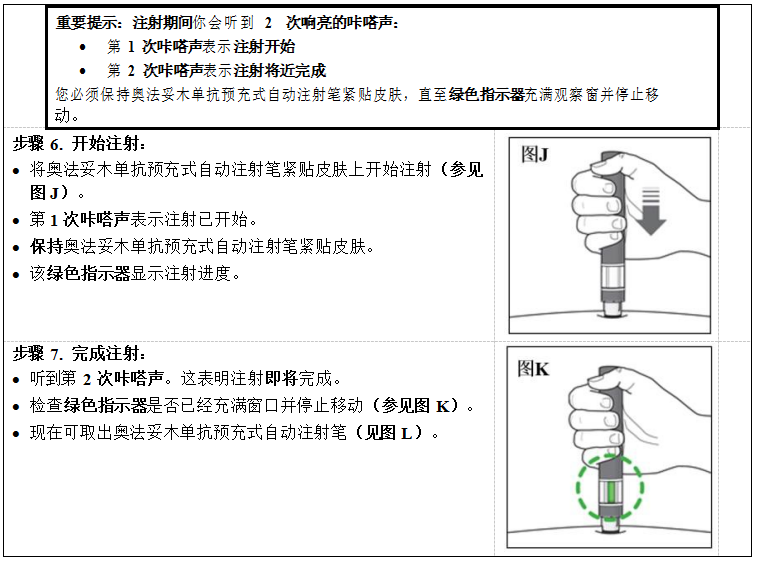
给药前,从冰箱中取出奥法妥木单抗预充式自动注射笔并放置 15 至 30 分钟,使之达到室温。在预充式注射液达到室温之前,请勿取下针盖。
在溶液和容器允许的情况下,应在给药前目视检查注射用药品是否存在颗粒物和变色。如果液体中含有可见异物或发生混浊,则请勿使用。
特殊人群
肾功能不全患者
尚未在肾功能不全患者中进行过奥法妥木单抗研究。
临床试验纳入了轻度肾功能不全患者。尚无在中度和重度肾功能不全患者中用药的经验。但是,由于奥法妥木单抗不经尿液排泄,预期肾损害患者不需要调整剂量(参见【药代动力学】)。
肝功能不全患者
尚未在肝功能不全患者中进行过奥法妥木单抗研究。
由于单克隆抗体(如奥法妥木单抗)的肝脏代谢可忽略不计,因此肝功能不全预期不会影响其药代动力学。因此,预计肝功能不全患者无需调整剂量(参见【药代动力学】)。



由于临床试验是在变化很大的条件下进行的,因此不能将在某种药物的临床试验中观察到的不良反应率直接与另一种药物的临床试验中观察到的不良反应率进行比较,并且可能无法反映临床实践中观察到的不良反应率。
在临床研究中,约有 1500 例 RMS 患者接受了奥法妥木单抗治疗。在研究 1 和研究 2 中,1882 例 RMS 患者被随机分组,其中 946 例接受奥法妥木单抗治疗,中位持续时间为85 周;33%接受奥法妥木单抗治疗的患者治疗时间长达 120 周 (参见【临床试验】)。奥法妥木单抗治疗患者发生 超过 10%的且频率高于特立氟胺治疗患者的最常见不良反应为上呼吸道感染、注射相关反应(全身性)、头痛和注射部位反应(局部)。在接受奥法妥木单抗治疗的患者中,最常见的停药原因是低免疫球蛋白 M(3.3%),在试验方案中定义为 IgM 低于正常值下限(LLN)10%。
表 1 总结了研究 1 和研究 2 中发生的药物不良反应。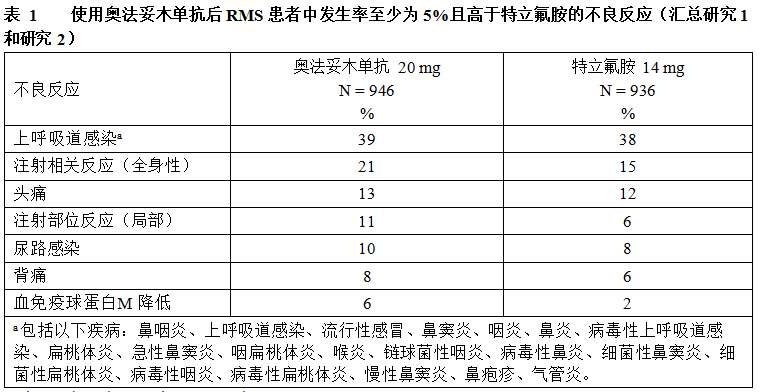
注射相关反应和注射部位反应
注射相关反应(全身性)的发生率在首次注射时最高(14.4%),后续注射时降低(第二次注射时为 4.4%,第三次注射时低于 3%)。注射相关反应的严重程度主要为轻度至中度(99.8%)。2 例(0.2%)接受奥法妥木单抗治疗的患者报告了严重注射相关反应。没有致命的注射相关反应。最常报告的症状(2%或以上)包括发热、头痛、肌痛、寒战和疲乏。除全身注射相关反应外,给药部位局部反应十分常见。局部注射部位反应的严重程度
均为轻度至中度。最常报告的症状(2%或以上)包括红斑、疼痛、瘙痒和肿胀(参见【注意事项】)。
实验室检查异常免疫球蛋白
在研究 1 和研究 2 中,在奥法妥木单抗治疗患者中观察到 IgM 平均水平降低,但与感染风险增加无关(参见【注意事项】)。在研究 1 和研究 2 的 14.3%患者中,奥法妥木单抗治疗导致血清 IgM 降低,达到低于 0.34 g/dL 的值。奥法妥木单抗治疗 48 周后平均 IgG 水平下降 4.3%,96 周后升高 2.2%。
免疫原性
与所有治疗性蛋白一样,本品可能具有免疫原性。抗体形成的检测高度依赖于方法的灵敏度和特异性。此外,试验中观察到的抗体(包括中和抗体)阳性发生率可能受多种因素影响,包括试验方法、样本处理、样本采集时间、合并用药和基础疾病。由于这些原因, 将下述研究中的抗体发生率与其他研究中的抗体发生率或与其他奥法妥木单抗产品进行比较可能会产生误导。
914 例奥法妥木单抗治疗患者中,2 例(0.2%)检测到治疗诱导的抗药抗体(ADA); 未发现患者存在导致治疗增强或中和的 ADA。阳性 ADA 滴度对任何患者的 PK、安全性特征或 B 细胞动力学均无影响;然而,这些数据不足以评估 ADA 对奥法妥木单抗安全性和有效性的影响。
奥法妥木单抗禁用于以下患者:
活动性 HBV 感染(参见【注意事项】)。
感染
在其他抗 CD20 B 细胞消耗疗法中观察到感染风险增加。
奥法妥木单抗有可能增加感染风险,包括严重细菌、真菌和新发或再激活的病毒感染; 其中一些感染在接受其他抗 CD20 抗体治疗的患者中具有致死性。在研究 1 和研究 2 (参见【临床试验】)中,接受奥法妥木单抗治疗的患者中感染和严重感染的总体发生率与接受特立氟胺治疗的患者相似(分别为 51.6% 比 52.7%和 2.5% 比 1.8%)。在针对复发型MS(RMS)患者的随机临床试验中,接受奥法妥木单抗治疗患者报告的最常见感染包括上呼吸道感染(39%)和尿路感染(10%)。活动性感染患者应延迟使用奥法妥木单抗,直到感染缓解。
与其他免疫抑制剂联用可能增加免疫抑制效应的风险
当在免疫抑制治疗后开始奥法妥木单抗治疗或在奥法妥木单抗治疗后开始免疫抑制治疗时,应考虑免疫抑制作用增加的可能性(参见【药物相互作用】和【药代动力学】)。尚未研究奥法妥木单抗与其他 MS 治疗的联合用药。
乙肝病毒
再激活
在接受奥法妥木单抗治疗的 MS 患者中未报告 HBV 再激活。然而,在接受奥法妥木单抗治疗慢性淋巴细胞白血病(CLL)的患者(静脉给药剂量高于 MS 的推荐剂量,但治疗持续时间较短)和接受其他抗 CD20 抗体治疗的患者中,发生过 HBV 再激活,在某些情况下可导致暴发性肝炎、肝衰竭和死亡。
感染
奥法妥木单抗禁用于活动性乙肝患者。在既往未感染过 HBV 的患者中,接受奥法妥木单抗治疗 CLL 的患者曾发生由 HBV 引起的致死性感染(静脉给药剂量高于 MS 的推荐剂量,但治疗持续时间较短)。在开始奥法妥木单抗治疗前,所有患者均应进行 HBV 筛查。筛查至少应包括乙肝表面抗原(HBsAg)和乙肝核心抗体(HBcAb)检测。根据当地指南,也可通过其他适当的标记物加以补充检测。对于 HBsAg 阴性且乙肝核心抗体阳性[HBcAb +] 或 HBV [HBsAg +] 的携带者,在开始奥法妥木单抗治疗前和治疗期间请咨询肝病专家。应按照当地医疗标准对这些患者进行监测和管理,以预防 HBV 感染或再激活。进行性多灶性脑白质病
进行性多灶性脑白质病(PML)是一种 JC 病毒(JCV)引起的脑部机会性病毒感染, 通常发生于免疫力受损的患者,并通常会导致死亡或重度残疾。
尽管在 RMS 临床试验中,奥法妥木单抗治疗患者中未报告 PML 病例,但在接受奥法妥木单抗治疗 CLL 的患者中发生了导致死亡的 PML(静脉给药剂量显著高于 MS 的推荐剂量,但治疗持续时间较短)。此外,在接受其他抗 CD20 抗体和其他 MS 治疗的患者中也观察到导致 PML 的 JCV 感染。在首次出现提示 PML 的体征或症状时,停用奥法妥木单抗并进行适当的诊断评价。在出现临床体征或症状之前,磁共振成像(MRI)结果可能已经很明显。与 PML 相关的典型症状多种多样,可在数天至数周内进展,包括身体一侧出现进行性无力或肢体笨拙、视力障碍以及思维、记忆和定向改变,从而导致意识模糊和人格改变。
如果确诊 PML,则应停止奥法妥木单抗治疗。
疫苗接种
对于活疫苗或减毒活疫苗,应在患者开始使用奥法妥木单抗治疗前至少 4 周根据免疫指南进行所有免疫接种,对于灭活疫苗,尽可能在患者开始使用奥法妥木单抗治疗前至少2 周根据免疫指南进行所有免疫接种。
奥法妥木单抗可能会干扰灭活疫苗的有效性。
尚未研究在奥法妥木单抗治疗后使用活疫苗或减毒活疫苗的免疫安全性。在治疗期间以及停药后其 B 细胞水平恢复正常之前,不建议接种活疫苗或减毒活疫苗(参见【药代动力学】) 。
妊娠期间使用奥法妥木单抗治疗的母亲所生婴儿的疫苗接种
对怀孕期间接受奥法妥木单抗治疗的母亲所生婴儿,在确认其 B 细胞计数恢复正常水平之前,不应接种活疫苗或减毒活疫苗。这些婴儿中 B 细胞的耗竭可能会增加活疫苗或减毒活疫苗的风险。
灭活疫苗可根据指征在 B 细胞耗竭恢复之前接种,但应考虑评估疫苗免疫应答,包括咨询有资质的专家,以确定是否产生保护性免疫应答。
注射相关反应
在研究 1 和研究 2 中,接受奥法妥木单抗治疗的患者分别有 21%和 11%报告了全身和局部注射反应,而接受特立氟胺治疗并接受匹配安慰剂注射的患者分别有 15%和 6%报告了全身和局部注射反应(参见【不良反应】和【临床试验】)。
在临床试验中观察到的伴有全身症状的注射相关反应最常发生在首次注射后 24 小时内,但在随后的注射中也观察到。观察到的症状包括发热、头痛、肌痛、寒战和疲乏,大部分患者(99.8%)为轻度至中度。RMS 临床试验中未发生危及生命的注射反应。
临床试验中观察到的局部注射部位反应症状包括红斑、肿胀、瘙痒和疼痛。
在 RMS 临床试验中仅观察到皮质类固醇、抗组胺药或对乙酰氨基酚预处理用药的有限获益。第一次注射奥法妥木单抗应在接受过相应培训的医疗保健专业人士的指导下进行。如果发生注射相关反应,则建议对症治疗。
免疫球蛋白减少
与任何 B 细胞消耗治疗的预期结果一致,观察到免疫球蛋白水平降低。在 RMS 临床试验中,7.7%接受奥法妥木单抗治疗的患者和 3.1%接受特立氟胺治疗的患者报告了免疫球
蛋白 M(IgM)降低 (参见【不良反应】)。3.4%接受奥法妥木单抗治疗的患者和 0.8%接受特立氟胺治疗的患者因免疫球蛋白降低而停止治疗。研究结束时未观察到免疫球蛋白 G
(IgG)下降。在治疗期间,尤其是机会性或反复感染患者中,以及停止治疗后,应监测定量血清免疫球蛋白的水平,直至 B 细胞水平恢复正常。如果免疫球蛋白较低的患者发生严重机会性感染或反复感染,或如果存在长期低丙球蛋白血症需要静脉注射进行免疫球蛋白治疗,则考虑停止奥法妥木单抗治疗。
胎儿风险
基于动物数据,奥法妥木单抗可因 B 细胞淋巴细胞减少造成胎儿伤害,并降低子宫内暴露于奥法妥木单抗的后代抗体反应。据报道,妊娠期间暴露于其他抗 CD20 B 细胞消耗抗体的母亲所生的婴儿中,观察到短暂性外周血 B 细胞耗竭和淋巴细胞减少症。建议有生育能力的女性在接受奥法妥木单抗期间和末次给药后至少 6 个月内采取有效的避孕措施
(参见【孕妇及哺乳期妇女用药】)。
RMS 临床试验中未报告用药过量的病例。
在 MS 患者的临床试验中,静脉给药剂量高达 700 mg 时未出现剂量限制性毒性。如果发生用药过量,建议监测患者的任何不良反应的体征或症状,必要时采取适当的对症治疗。
尚无关于妊娠期女性使用奥法妥木单抗相关发育风险的充分数据。根据动物研究的结果,奥法妥木单抗可能会穿过胎盘屏障并导致胎儿 B 细胞耗竭。 据报道,妊娠期间暴露于其他抗 CD20 抗体的母亲所生的婴儿中,观察到短暂性外周血 B 细胞耗竭和淋巴细胞减少。尚未在临床试验中研究母体暴露于奥法妥木单抗后婴儿的B 细胞水平。尚不清楚宫内暴露于奥法妥木单抗的婴儿中 B 细胞耗竭的潜在持续时间,以及 B 细胞耗竭对疫苗安全性和有效性的影响。在 B 细胞恢复之前应避免对宫内暴露于奥法妥木单抗的新生儿和婴儿接种活疫苗(参见【注意事项】和【药代动力学】)。 妊娠猴接受奥法妥木单抗给药后,在血浆水平显著高于人类的情况下,在后代中观察到死亡率增加、B 细胞群耗竭和免疫功能受损,但无母体毒性。 在美国普通人群中,临床确认的妊娠中重大出生缺陷和流产的估计背景风险分别为2%- 4%和 15% - 20%。尚不清楚适应症人群发生重大出生缺陷和流产的背景风险。 有生育能力的女性和男性 有生育能力的女性在接受奥法妥木单抗期间和最后一次使用奥法妥木单抗治疗后的 6 个月内应采取有效的避孕方法(参见【注意事项】和【药代动力学】)。尚无关于人乳汁中存在奥法妥木单抗、对母乳喂养婴儿的影响或药物对乳汁生成影响的数据。人 IgG 可经人乳汁分泌,尚不清楚吸收奥法妥木单抗导致婴儿 B 细胞耗竭的可能性。应当考虑母乳喂养对发育和健康的好处,以及母亲对奥法妥木单抗的临床需求以及奥法妥木单抗对母乳喂养的新生儿/婴儿的任何潜在不利影响。尚未确定在儿科患者中的安全性和有效性。在奥法妥木单抗的临床试验中,未纳入充足数量的老年患者,因此无法确定老年患者的反应是否与年轻受试者有所不同。
免疫抑制或免疫调节疗法
奥法妥木单抗与免疫抑制剂药物(包括全身性皮质类固醇)合并使用可能增加感染风险。当奥法妥木单抗与免疫抑制疗法联合使用时,应考虑免疫系统效应累加的风险。
在转换具有免疫效应的药物时,应考虑到这些药物的作用时间和作用机制,因为同时启动奥法妥木单抗治疗可能会产生额外的免疫抑制作用。
Novartis Pharma Stein AG
86979584000051
奥法妥木单抗治疗多发性硬化症的确切机制尚不清楚,但被认为与 CD20 的结合有关。CD20 是一种表达于前 B 淋巴细胞和成熟 B 淋巴细胞的细胞表面抗原。奥法妥木单抗在细胞表面与 B 淋巴细胞结合后,可导致抗体依赖性的细胞溶解以及补体介导的溶解。
遗传毒性
奥法妥木单抗未进行遗传毒性研究。奥法妥木单抗作为抗体药物,预期不会直接与
DNA 发生相互作用。生殖毒性
猴静脉注射给予奥法妥木单抗(前 5 周每周一次,剂量为 10 和 100 mg/kg,随后每 2
周一次,剂量为 3 和 20 mg/kg),对雄性和雌性生殖参数(包括激素、月经周期、精子分析或生殖器官的组织病理学评价)未见影响。猴高剂量下的血浆暴露量(Cave)为人推荐维持剂量(20mg/月)的 500 倍以上。
猴于器官发生期间(妊娠第 20 至 50 天)静脉注射奥法妥木单抗(每周一次,剂量为
20 或 100 mg/kg)未见对胚胎/胎仔发育的不良影响;但在妊娠第 100 天评价时,两个剂量下均可见胎仔 B 细胞耗竭。胚胎/胎仔发育无影响剂量(100 mg/kg)下的血浆暴露量(Cave) 为推荐人维持剂量(20 mg)的 5000 倍以上。未确定对 B 细胞的无影响剂量,低影响剂量
(20 mg/kg)下的血浆暴露(Cave)约为人推荐维持剂量(20 mg/月)的 780 倍。
猴在整个妊娠期间静脉注射奥法妥木单抗(前 5 周每周一次,剂量为 10 和 100 mg/kg,
随后每 2 周一次,剂量为 3 和 20 mg/kg)未见对子代发育的不良影响,但是,高剂量下子代可见出生后死亡、B 细胞耗竭和免疫功能受损。高剂量下的子代死亡被认为继发于 B 细胞衰竭。发育毒性的未见不良影响剂量(100/20 mg/kg)下,母体的血浆暴露量(Cave)约为人推荐维持剂量的 500 倍。由于低剂量组可评价的子代数量有限,未能确定子代死亡及免疫功能的无影响剂量。
致癌性
奥法妥木单抗未进行致癌性研究。
在两项设计相同的随机、双盲、双模拟、活性药物对照临床试验中,在复发型 MS 患者中证实了奥法妥木单抗的疗效 [研究 1(NCT02792218)和研究 2(NCT02792231)]。两项研究均入组了前一年至少复发 1 次、前 2 年复发 2 次或前一年存在 T1 钆增强(GdE)病灶的患者。还要求患者的扩展残疾状态量表(EDSS)评分为 0-5.5。
患者随机接受奥法妥木单抗,第 1、7 和 14 天 20 mg 皮下给药,随后从第 4 周开始 20
mg 每 4 周一次,同时每日口服安慰剂,或口服活性对照药物特立氟胺,剂量为 14 mg,每日一次,同时在第 1、7、14 天皮下给予安慰剂,此后每 4 周一次。单个患者的治疗持续时
间因何时达到研究结束标准而异。单个患者的最长治疗持续时间为 120 周。在基线、设盲治疗期间每 3 个月和疑似复发时进行神经学评价。在基线、1 年和 2 年时进行脑 MRI 扫描。
两项试验的主要终点是治疗期间的年复发率(ARR)。其他结局指标包括:1)汇总人群中至 3 个月确认残疾进展的时间;2)第 48 和 96 周扫描的 T1 GdE 病灶数量,以及 3) T2 新发或增大 MRI 病灶的年化发生率。残疾进展定义为基线 EDSS 为 0、1 - 5 或 5.5 或以上的患者 EDSS 分别增加至少 1.5、1 或 0.5 分。
在研究 1 中,共有 927 例患者随机接受奥法妥木单抗(n = 465)或特立氟胺(n = 462)。在随机分配至奥法妥木单抗组的患者中,90%完成了该研究;在随机分配至特立氟胺组的患者中,81%完成了该研究。各治疗组间的人口统计学和疾病特征保持均衡。平均年龄为38 岁,89%为白人,69%为女性。自 MS 诊断的平均时间为 5.7 年,基线时的中位 EDSS 评分为 3.0;60%的患者接受过类固醇以外的 MS 药物治疗。基线时,前一年的平均复发次数为 1,MRI 扫描显示的 T1 GdE 病灶的平均数量为 1.5。
在研究 2 中,共有 955 例患者随机接受奥法妥木单抗(n = 481)或特立氟胺(n = 474)。在随机分配至奥法妥木单抗组的患者中,83%完成了该研究;在随机分配至特立氟胺组的患者中,82%完成了该研究。各治疗组间的人口统计学和疾病特征保持均衡。平均年龄为38 岁,87%为白人,67%为女性。自 MS 诊断的平均时间为 5.5 年,基线时的中位 EDSS 评分为 2.5;61%的患者接受过类固醇以外的 MS 药物治疗。基线时,前一年的平均复发次数为 1.3,MRI 扫描显示的 T1 GdE 病灶的平均数量为 1.6。
在两项研究中,与特立氟胺相比,奥法妥木单抗显著降低了 ARR。
与特立氟胺相比,奥法妥木单抗显著降低了 3 个月确认残疾进展风险。
在两项研究中,奥法妥木单抗显著减少了 T1 GdE 病灶的数量和新发或增大的 T2 病灶的比率。
研究 1 和研究 2 的关键结果见表 2 和图 1。
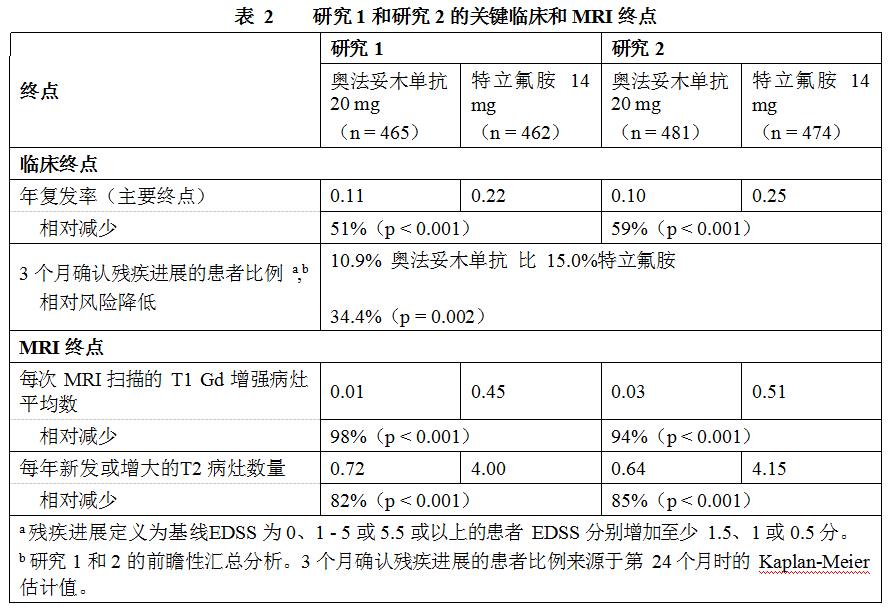
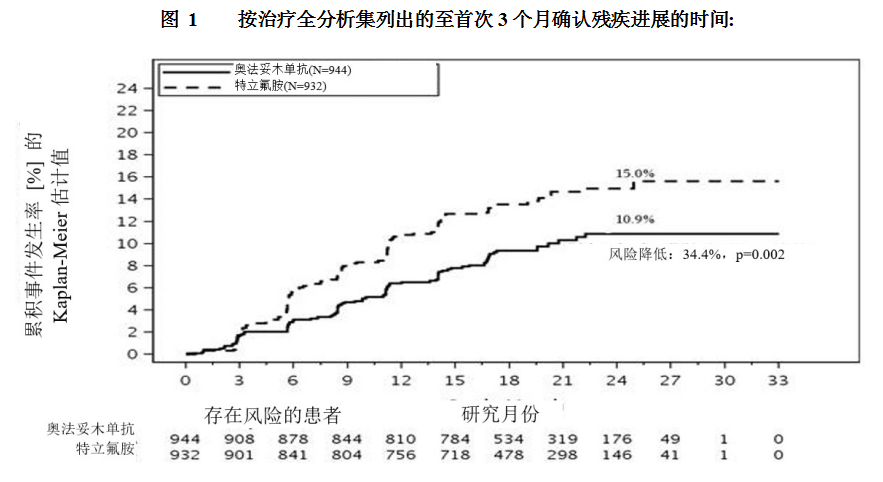
在按性别、年龄、体重、既往非类固醇类 MS 治疗以及基线残疾和疾病活动度定义的探索性亚组中,在两项研究中观察到奥法妥木单抗相对于特立氟胺对关键疗效结果的效果在各亚组中相似。
药效动力学
B 细胞耗竭
使用 CD19+B 细胞试验用于 B 细胞计数,因为奥法妥木单抗的存在会干扰 CD20 分析。在研究 1 和研究 2 中,奥法妥木单抗按推荐给药,治疗开始后 1 周分别有 77.0%和 78.8% 的患者CD19+B 细胞降至LLN 以下,治疗开始后 2 周分别有 95.0%和 95.8%的患者CD19+B 细胞降至 LLN 以下(参见【用法用量】和【临床试验】)。在研究 1 和研究 2 中,第 12 周时,99.3% - 99.5%的患者 CD19+B 细胞计数低于 LLN。在奥法妥木单抗治疗期间,从 12 周至 120 周,研究 1 中约 97%的患者和研究 2 中 92%的患者的 CD19+B 细胞计数保持低于LLN。
在一项使用与研究 1 和研究 2 相同给药方案的生物等效性研究中,在开始维持治疗期之前,94%的患者在第 4 周和 98%的患者在第 12 周总 CD19+B 细胞水平低于规定的阈值10 个细胞/µL。
B 细胞恢复
来自 RMS 临床试验的数据表明,在停药后 24 至 36 周内,至少 50%的患者的 B 细胞恢复超过 LLN。B 细胞恢复的建模和模拟确证了该数据,预测 B 细胞恢复的中位时间为停药后 40 周。
药代动力学吸收
20 mg 每 4 周一次皮下给药导致稳态时平均 AUCtau 为 483 μg•h/ml,平均 Cmax 为 1.43 μg/ml。
皮下给药后,与其他治疗性单克隆抗体相似,奥法妥木单抗被认为主要通过淋巴系统吸收。
分布
奥法妥木单抗 20 mg 重复皮下给药后,稳态分布容积估计为 5.42L。
消除
代谢
奥法妥木单抗是一种蛋白质,其代谢途径预期是经普遍存在的蛋白水解酶降解为小肽和氨基酸。
排泄
奥法妥木单抗可以通过两条途径消除:一条与其他 IgG 分子一样的靶标非依赖性途径, 另一条是与 B 细胞结合相关的靶标介导途径。在治疗开始时,基线 B 细胞计数越高,靶点介导的消除清除成分越多,奥法妥木单抗的半衰期越短。B 细胞耗竭后,重复皮下给予奥法妥木单抗 20 mg 注射液后,清除率估计为 0.34 L/天。奥法妥木单抗 20 mg 重复皮下给
药后,稳态半衰期估计约为 16 天。特殊人群
以下群体特征对奥法妥木单抗的药代动力学不具有临床意义的影响:体重、性别、年龄、人种或基线 B 细胞计数。
肾/肝功能不全患者
尚未在肾或肝功能不全患者中研究奥法妥木单抗的药代动力学。药物相互作用研究
奥法妥木单抗与经过细胞色素 P450 系统或其他药物代谢酶代谢的化学药物没有共同的清除途径。此外,没有证据表明 CD20 单克隆抗体参与药物代谢酶表达的调节。尚未对奥法妥木单抗与其他药物之间的相互作用开展正式研究。
遗传药理学
不适用
注射剂
20mg(0.4mL)/支
奥法妥木单抗注射液装在一次性玻璃注射器中,该注射器配有不锈钢针头、柱塞和硬质针头护套,溶液量为 0.4 mL。注射器已被装配到预充式自动注射笔中。 包装规格:每盒 1 支(预充式自动注射笔)。
在 2 °C - 8 °C 下保存和运输,不得冷冻。请将本品置于原包装盒中以避光保存直至使用。为避免起泡,请勿振摇。
24 个月
国药准字SJ20210034

