普罗力说明书
Denosumab Injection
地舒单抗
活性成份:地舒单抗(RANK 配体的免疫球蛋白 G2 全人源单克隆抗体)。 辅料:冰醋酸、氢氧化钠、山梨醇、聚山梨酯 20 和注射用水。
普罗力地舒单抗注射液为预充于注射器中的澄清、无色至淡黄色液体
用于骨折高风险的绝经后妇女的骨质疏松症。 在绝经后妇女中,本品可显著降低椎体、非椎体和髋部骨折的风险。
本品的推荐剂量为 60 mg,单次皮下注射,每 6 个月给药一次,注射部位为大腿、腹部或上臂部。 患者必须充分补充钙和维生素 D(见【注意事项】)。 尚未确定接受骨质疏松症抗骨吸收治疗(包括地舒单抗和双膦酸盐)的最佳总治疗时间。 应基于个体患者的风险获益比,定期评估是否需要继续治疗,尤其是接受 5 年及以上治疗后(见 【注意事项】)。 肾功能损害患者 肾功能损害患者不需要调整剂量(见【注意事项】中与钙监测相关的推荐意见)。 肝功能损害患者
尚未在肝功能损害患者中研究地舒单抗的安全性和有效性(见【药代动力学】)。 老年用药(年龄 ≥ 65 岁) 老年患者不需要调整剂量。 <u>给药途径</u> 皮下给药,应由医务人员实施。
在给药前应检查溶液。如果含有颗粒、浑浊或变色,请勿注射。本品禁止摇晃。为避免注射部位不适,应在注射前使预充式注射器达到室温(最高 25°C),并缓慢注射。请注射预充式注射器中的全部药液。 应该按照当地有关规定处理任何未使用的药品或废弃物。 因为未开展相容性研究,本品禁止与其他药品混合 。
(
对活性成份或任何辅料成份(见 【成份】)过敏者禁用。 低钙血症(见【注意事项】)
<u>补充钙和维生素 D</u> 对于所有患者, 摄入足够的钙和维生素 D 至关重要。 <u> 使用注意事项</u> 低钙血症 识别存在低钙血症风险的患者至关重要。在开始治疗前必须通过摄入足够的钙和维生素 D 来纠正低钙血症。推荐在每次给药前, 以及在易于出现低钙血症的患者第一次给药后 2 周内对其钙水平进行临床监测。如果任何患者在治疗期间出现低钙血症疑似症状(见 【不良反应】), 应测定钙水平。应鼓励患者报告提示低钙血症的症状。 已有上市后重度症状性低钙血症的报告(见 【不良反应】),多数病例在治疗开始后 的最初数周内出现,但也可在更晚时间发生。 糖皮质激素合并治疗也是导致低钙血症的额外危险因素。 肾功能损害
重度肾功能损害患者(肌酐清除率 < 30 ml/min)或接受透析的患者发生低钙血症的风险更高。随着肾功能损害程度的加重,低钙血症伴甲状旁腺素水平升高的风险增加。所以,摄入足够的钙、维生素 D 和定期监测钙水平对这类患者尤其重要。 皮肤感染 接受本品治疗的患者可能会发生导致住院的皮肤感染(主要为蜂窝织炎)(见 【不良反应】)。如果出现蜂窝织炎的症状和体征,建议患者马上就医。 颌骨坏死(ONJ) 在因骨质疏松症而接受本品治疗的患者中罕有 ONJ 报告(见【不良反应】)。 口腔内有未愈合的开放性软组织病变的患者应推迟开始治疗/新疗程的时间。对于存在 合并危险因素的患者,建议在开始地舒单抗治疗前进行预防牙科检查和个体获益/风险评估。 在评估患者发生 ONJ 的风险时应考虑以下危险因素: 药品抑制骨质吸收的能力(抑制能力越强,风险越高)、给药途径(胃肠外给 药的风险更高)和抗骨吸收治疗药物的累积剂量。 - 肿瘤、合并症(例如贫血、凝血障碍、感染)、吸烟。 - 合并治疗:皮质类固醇、化疗、血管生成抑制剂、头颈部放疗。 - 口腔卫生不佳、牙周疾病、义齿契合度不佳、牙病史、侵入性牙科手术(例如 拔牙)。鼓励所有患者在地舒单抗治疗期间保持良好的口腔卫生、接受常规口腔检查和立刻报告任何口腔症状(例如牙齿活动、疼痛或肿胀、口腔溃疡不愈合或分泌物)。治疗期间,仅应在慎重考虑后行侵入性牙科手术,并应避免邻近本品给药时间。 治疗医师应与具有 ONJ 治疗经验的牙医或口腔外科医师密切合作,制定发生 ONJ 患者的管理计划。如可行,应考虑暂时中断治疗,直到病症消退和相关危险因素缓解。 外耳道骨坏死 地舒单抗已有外耳道骨坏死的报告。外耳道骨坏死的可能危险因素包括使用类固醇和化疗和/或局部危险因素(例如感染或创伤)。在接受地舒单抗治疗且出现耳部症状(包括慢性耳部感染)的患者中,应考虑发生外耳道骨坏死的可能性。 非典型股骨骨折 在接受地舒单抗治疗的患者中已有发生非典型股骨骨折的报告(见 【不良反应】)。非典型股骨骨折可在几乎没有创伤的情况下发生在转子下和股骨干区域。这些事件有特定影像学表现。在某些合并症患者中(例如维生素 D 缺乏、类风湿性关节炎、低磷酸酶血症)和使用特定药物(例如双膦酸盐、皮质类固醇、质子泵抑制剂)的患者中也已有非典型股骨骨折的报告。这些事件也曾在未接受抗骨吸收药物治疗的情况下发生。所报告的与双膦酸盐相关的类似骨折通常为双侧;因此发生股骨干骨折且接受地舒单抗治疗的患者应检查对侧股骨。在对疑似有非典型股骨骨折的患者进行基于个体获益风险评估之前,应考虑中断本品治疗。在地舒单抗治疗期间,建议患者报告新发或不寻常的股部、髋部或腹股沟疼痛。应评估出现此类症状的患者有无不完全股骨骨折。 终止本品治疗后多发性椎体骨折 (MVF) 在终止本品治疗后可能会发生多发性椎体骨折 (MVF),特别是对于有椎体骨折史的 患者。建议患者在没有医生建议的情况下不要中断本品治疗。在终止本品治疗前应评估个体获益/风险。如果终止本品治疗,应考虑改用另外一种抗骨吸收的治疗药物。 长期抗骨吸收治疗 长期抗骨吸收治疗(包括地舒单抗和双膦酸盐)可能导致不良结局的风险增加,例如显著抑制骨重建引起的颌骨坏死和非典型股骨骨折(见 【用法用量】)。 使用其他含地舒单抗制剂的合并治疗 正在接受本品治疗的患者不应接受其他含地舒单抗的药物的合并治疗(预防成人实体瘤骨转移的骨骼相关事件)。辅料警告 本品每毫升溶液含有 47 mg 山梨醇。应考虑合并接受含山梨醇(或果糖)产品及饮食摄 入山梨醇(或果糖)的叠加效应。 本品每 60 mg 含钠量低于 1 mmol(23 mg),即基本上“无钠”。 本品对驾驶车辆和使用机械的能力没有影响或影响可忽略。
尚无孕妇使用地舒单抗的数据或数据尚不充分。孕妇和有生育能力且未进行避孕的女性 禁用本品。动物研究表明本品具有生殖毒性(见 【药理毒理】)。建议女性患者避免在接受本品治疗期间及治疗结束后至少 5 个月内怀孕。由于单克隆抗体透过胎盘转运会随着妊娠的进展逐渐增加,妊娠晚期的量最大,因此本品的任何效应可能在妊娠中期和晚期更大。 尚不清楚地舒单抗能否经人乳分泌。由于本品可能会对哺乳婴儿导致不良反应,应决定 停止哺乳,还是停止本品治疗。应权衡哺乳对新生儿/婴儿获益以及本品治疗对女性患者的获益,然后决定停止哺乳,还是停止本品治疗。
Amgen Manufacturing Limited
86982980000013
地舒单抗可与核因/子-κB 受体活化因子配体(RANKL)结合。RANKL 是一种对破骨细 胞的形成、功能和存活发挥关键作用的跨膜或可溶性蛋白。破骨细胞在体内负责骨吸收。地舒单抗能够阻断 RANKL 激活`破骨细胞及其前体表面的受体 RANK,阻断 RANKL/RANK 相互作用可抑制破骨细胞形成、功能和存活,从而减少骨吸收,增加骨皮质和骨小梁的骨量和强度。
重复给药毒性:30~48 月龄/食蟹猴(相当于人类青少年)皮下注射地舒单抗 1、10、50 mg/kg,每 4 周 1 次,连续 12 个月,在 10、50 mg/kg 剂量下,食蟹猴股骨、胫骨、胸骨出现药物相关性改变,包括骨骺生长板增大、该区域软骨破裂`降低,破骨细胞和成骨细胞减少。50 mg/kg 剂量下未见对雄性动物生育力的明显影响。各剂量组动物均检测到高比例的阳性抗药抗体,导致药物清除率升高、药理活性下降,未见免疫复合物沉积。本试验 NOAEL 值为 50 mg/kg(按 mg/kg 计算,高于人体推荐剂量 60 mg 的 50 倍)。遗传毒性:尚未开展地舒单抗的遗传毒性研究。生殖毒性:雌性食蟹猴自交配前两个月经周期至交配后 20 天,每周 1 次,连续皮下注射地舒单抗最高达 12.5 mg/kg(按 mg/kg 计算,高于人体推荐剂量 60 mg 的 13 倍),未见对雌性动物生育力的不良影响。食蟹猴自妊娠 20 至 50 日,每周 1 次连^续皮下注射地舒单抗 2.5、5、12.5 mg/kg,未引起母体毒性、发育毒性或致畸性作用。食蟹猴自妊娠 20 日至分娩,每月 1 次皮下注射地舒单抗 50 mg/kg(按 mg/kg 计算,高于人体推荐剂量的 50 倍),妊娠期流产、死胎、产后死亡率升高,幼仔生长缓慢,腋窝、腹股沟、下颌及肠系膜淋巴结缺失,骨骼生长异常、骨强度降低、造血功能下降、牙齿发育不良、牙齿排列不齐。从出生至 1 月龄,幼仔体内可检测到地舒单抗,浓度为母体水平的 22~621%。幼仔从出生至 6 月龄恢复期时,骨质及骨骼强度可恢复正常,对牙齿萌出未见不良影响,但仍存在牙齿发育不良及髓外造血;腋窝和腹股沟淋巴结仍缺失,下颌及肠系膜淋巴结可见,但体积小;在恢复期 1 只动 物中,观察到多种组织的微小至中度矿化。分娩前未见对母体的损害,分娩期间母体的不良反应发生不频繁。产后 14 天(距最后给药日 1 个月)母体乳汁中可检测到地舒单抗,乳汁/母体血清比为 0.48%。母体乳腺发育正常。由于本试验仅 50 mg/kg 单一剂量,因此未确定胎仔 NOAEL 值。在子宫内暴露于地舒单抗的雌性幼仔,在 6 月龄时乳腺病理学检查未见异常,但对幼仔发育及泌乳未进行充分评估。致癌性:尚未在动物中开展地舒单抗的长期致癌性研究。
<u>在绝经后骨质疏松症妇女中的临床有效性和安全性</u> 在绝经后骨质疏松症妇女中开展的全球 III 期有效性和安全性研究 在基线腰椎或全髋骨密度(BMD)T 评分在 -2.5 和-4.0 之间,且主要骨质疏松性骨折与髋部骨折 10 年平均绝对骨折概率分别为 18.60%(十分位数:7.9-32.4%)和 7.22%(十分位数:1.4-14.9%)的绝经后妇女(7808 名年龄 60-91 岁的妇女,其中 23.6% 具有再发性椎体骨折)中研究了本品每 6 个月给药一次,连续治疗 3 年时的有效性和安全性。患有其他疾病或接受可能影响骨骼的治疗的女性被排除在本项研究之外。女性患者每天补充钙(至少 1000 mg)和维生素 D(至少 400 IU)。 对椎体骨折的影响 在治疗的第 1、2 和 3 年,本品可显著降低新发椎体骨折风险(p < 0.0001)(见表 2)。 表 2.地舒单抗对新发椎体骨折风险的影响
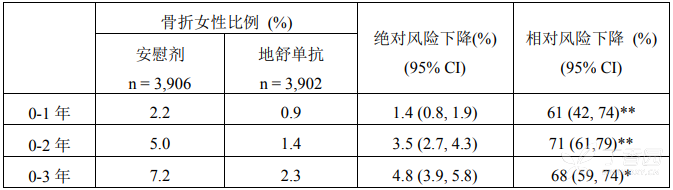
p < 0.0001, *p < 0.0001 – 探索性分析 对髋部骨折的影响 接受地舒单抗治疗 3 年后,髋部骨折风险相对下降了 40%(绝对风险下降 0.5%)(p < 0.05)。在第 3 年,安慰剂组髋部骨折发生率为 1.2%,地舒单抗组为 0.7%。 在一项针对 > 75 岁妇女的事后分析中,地舒单抗组的相对风险下降了 62%(绝对风险下降 1.4%,p < 0.01)。 对所有临床骨折的影响 本品可显著降低所有类型/组别的骨折(见表 3)。 表 3. 第 3 年地舒单抗对临床骨折风险的影响
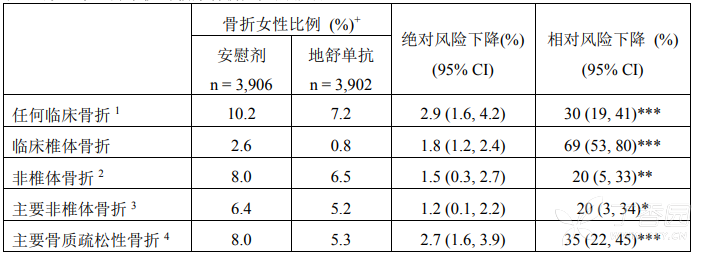
p ≤ 0.05; p = 0.0106(包含在多重性校正中的次要终点),p ≤ 0.0001 + 基于 3 年 Kaplan-Meier 估计值的事件发生率。 1 包括临床椎体骨折和非椎体骨折。 2 不包括椎体、颅骨、面部、下颌、掌骨和手指指骨与足趾趾骨骨折。 3 包括骨盆、股骨远端、胫骨近端、肋骨、肱骨近端、前臂和髋部骨折。 4 根据 WHO 定义,包括临床椎体、髋部、前臂和肱骨骨折。在基线股骨颈 BMD ≤ -2.5 的妇女中,本品可降低非椎体骨折风险(相对风险下降 35%,绝对风险下降 4.1%,p < 0.001,探索性分析)。 无论 10 年基线骨折风险如何,本品 3 年内新发椎体骨折、髋部骨折和非椎体骨折的发生率均一致降低。 对骨密度的影响 在治疗第 1、2 年 3 年,与安慰剂相比,地舒单抗组中所有测量的临床部位的 BMD 均升高。在第 3 年,地舒单抗组腰椎 BMD 升高 9.2%,全髋 BMD 升高 6.0%,股骨颈 BMD 升高 4.8%,髋部转子 BMD 升高 7.9%,桡骨远端 1/3 处 BMD 升高 3.5%,全身 BMD 升高 4.1%(均 p < 0.0001)。 在观察停止地舒单抗治疗后的影响的临床研究中,BMD 在末次给药后 18 个月内大致恢 复至治疗前水平,并保持高于安慰剂组。这些数据表明地舒单抗需要连续治疗方可维持治疗作用。重新开始地舒单抗治疗可使 BMD 升高,且与首次治疗时相似。 治疗绝经后骨质疏松症的开放标签扩展研究 共 4550 名在上述关键性研究中错过试验用药给药不超过 1 次并完成了第 36 个月研究访视的妇女(地舒单抗组 2343 名,安慰剂组 2207 名)同意入组这项 7 年、多国、多中心、开放标签、单组、扩展研究来评价地舒单抗的长期安全性和有效性。在扩展研究中,所有女性患者每 6 个月接受一次地舒单抗 60 mg 治疗,同时每天补充钙(至少 1 g)和维生素 D(至少 400 IU)。共有 2626 名受试者(扩展研究中 58% 的女性,即关键研究中 34% 的女性)完成本项扩展研究。 在接受地舒单抗治疗长达 10 年的患者中,与关键研究的基线相比,腰椎的 BMD 升高 21.7%,全髋 BMD 升高 9.2%,股骨颈 BMD 升高 9.0%,转子 BMD 升高 13.0%, 桡骨远端 1/3 处 BMD 升高 2.8%。在接受 10 年治疗的患者中,研究结束时平均腰椎 BMD T 评分为 1.3。 将骨折发生率作为安全性终点进行了评估,由于终止治疗的患者数量较多且为开放标签研究设计,因此无法评估对骨折预防的有效性。在接受地舒单抗治疗 10 年的患者(n = 1278)中,新发椎体和非椎体骨折的累计发生率分别约为 6.8% 和 13.1%。因任何原因而未能完成研究的患者的治疗期间骨折发生率升高。
在扩展研究中发生了 13 例经裁定的颌骨坏死(ONJ)和 2 例经裁定的非典型股骨骨折。 <u>绝经后骨质疏松症妇女的骨组织学</u> 在地舒单抗治疗 1-3 年后评价了 62 名未接受过骨质疏松症治疗或从既往阿仑膦酸钠治 疗转换为本品治疗的骨质疏松症或低骨量绝经后妇女的骨组织学。59 名妇女在绝经后骨质疏松症扩展研究第 24 个月(n = 41)和/或第 84 个月(n = 22)参与了骨活检研究。骨活检结果显示:骨骼的结构和质量正常,未见矿化缺陷、编织骨或骨髓纤维化证据。绝经后骨质疏松症妇女的扩展研究中进行的组织形态学检测结果显示了地舒单抗的抗骨吸收作用(通过激活频率和骨形成速率来衡量)可随时间的延长而持续存在。
吸收 皮下注射 1.0 mg/kg 剂量(大/约相当于批准剂量 60 mg)后,基于 AUC 的暴露量为相 同剂量水平静脉给药时的 78%。皮下注射 60 mg 剂量后,在第 10 天(范围 2-28 天)达到最大血清地舒单抗浓度(Cmax),Cmax 为 6 μg/ml(范围 1-17 μg/ml)。生物转化 地舒单抗`仅由氨基酸和碳水化合物组成,为天然免疫球蛋白,不太可能经肝脏代谢机制 清除。预计地舒单抗的代谢和清除与免疫球蛋白的清除途径相同,可降解为小肽和单个氨基酸。清除 在达到 Cmax 后,血清水平在 3 个月(范围:1.5-4.5 个月)内逐渐下降,半衰期为 26 天(范围:6-52 天)。53% 患者在给药后 6 个月时无法检测到地舒单抗。 60 mg 每 6 个月一次多次给药后,未观察到地舒单抗的累积或药代动力学特征随时间推移的变化。地舒单抗结合抗体的产生对地舒单抗的药代动力学无影响,且男性与女性之间的药代^动力学相似。年龄(28 至 87 岁)、人种和疾病状态未显示对地舒单抗的药代动力学有显著影响。 基于 AUC 和 Cmax,观察到了体重越大则暴露量越小的趋势。但基于骨转换标志物和 BMD 升高药效学作用在较宽的体重范围内是一致的,该趋势被认为无临床重要意义。线性/非线性 在剂量探索研究中,地舒单抗的药代动力学呈非线性、剂量依赖性。剂量或浓度越高,清除率越低,但剂量大于等于 60 mg 时,暴露量大致以与剂量成比例的方式增高。 肾功能损害 在一项针对 55 名不同肾功能程度患者(包括接受透析的患者)的研究中,肾功能损害程度对地舒单抗的药代动力学无影响。 肝功能损害 未专门在肝功能损害患者中进行研究。一般而言,单克隆抗体不经肝代谢机制清除。预计肝功能损害对地舒单抗的药代动力学无影响。
注射剂
60mg(1.0ml)/支(预充式注射器)
以单剂量西林瓶供应。
2℃-8℃冰箱内保存,请勿冷冻。在原纸盒包装中,避光保存
624.00起
36 个月
S20200019
)

