新力莱说明书
Ravidasvir Hydrochloride Tablets
盐酸拉维达韦
本品主要成份为盐酸拉维达韦。
化学名称:甲基 N-[(2 S-1-[(2 S-2-[5-(6-{2-[(2 S)-1-(2 S)-2-(甲氧羰基)氨基]-3 甲基丁酰基]吡咯烷-2-基-1 H-1,3-苯并二唑-6-基}萘酚-2-基)-1 H-咪唑-2-基]吡咯烷-1-基]-3-甲基-1 氧代丁-2-基]氨基甲酸甲酯二盐酸盐
化学结构式:

分子式:C42H50N8O6·2HCI
分子量:835.82
盐酸拉维达韦片联合利托那韦强化的达诺瑞韦钠片和利巴韦林,用于治疗初治的基因 1b 型慢性丙型肝炎病毒感染的非肝硬化成人患者。
盐酸拉维达韦片不得作为单药治疗。
推荐剂量
本品口服,可空腹或与食物同服。
本品用法用量: 每次 200 mg,每日 1 次,连续 12 周。服用本品时须同时应用达诺瑞韦钠片、利托那韦和利巴韦林。
推荐达诺瑞韦钠片用法用量: 口服,每次 100 mg,每日 2 次;连续 12 周(详见达诺瑞韦钠片说明书)。
推荐利托那韦(RTV)用法用量: 口服,每次 100 mg,每日 2 次,连续 12 周(详见利托那韦片说明书)。
推荐利巴韦林用法用量:利巴韦林的剂量根据体重确定。如体重<75 kg,每次 500 mg,每日 2 次;如体重 ≥ 75 kg,每次 600 mg,每日 2 次;连续 12 周(详见利巴韦林制剂说明书)
剂量调整、暂停给药和停止治疗
不建议调整盐酸拉维达韦片的剂量,并应避免暂停给药。但如果因不良反应需要暂停给药联合治疗方案中的任何一种药物,则不得单独应用盐酸拉维达韦片治疗。
本品口服,可空腹或与食物同服。
本品禁用于既往对本品或本品中任何成份过敏的患者。
本品与其他药物联合使用时的禁忌,请参考相应药物的说明书。
乙型肝炎病毒再激活的潜在风险
在应用直接抗病毒药物治疗丙型肝炎的过程中及治疗后, 有乙型肝炎病毒(HBV)再激活的病例报告, 包括死亡病例。在开始治疗前, 所有患者均应进行 HBV 筛查。HBV/HCV 合并感染的患者存在 HBV 再激活的风险,所以应按照当前临床指南要求进行监测和治疗。
血液系统
本品联合治疗方案中与利巴韦林联用,应注意可能发生的贫血、中性粒细胞减少、白细胞减少和血小板减少。使用本品 + 达诺瑞韦钠片 + 利托那韦 + 利巴韦林治疗方案的临床研究中最常见的不良反应为贫血,发生率 39.62%(见【不良反应】),血红蛋白通常在给药后开始降低,最大平均降幅 24.15 g/L,一般不需要处理或者部分受试者调整利巴韦林剂量后,血红蛋白平均值在治疗结束后可恢复至正常范围。可能与联合治疗方案中利巴韦林的使用相关。
建议在该方案使用过程中定期监测血常规,发现血红蛋白过低应及时采取措施。对于已有贫血或有贫血风险的患者慎用。
联合用药
本品与利托那韦强化的达诺瑞韦钠片和利巴韦林联用时注意事项,见达诺瑞韦钠片、利托那韦和利巴韦林的说明书。
尚无本品用于妊娠妇女的数据。动物实验显示本品有潜在致畸作用(见【药理毒理】),但对人类的潜在危险性未知。不建议妊娠期妇女使用本品。本品尚不清楚本品及其赋型剂是否经人乳分泌,因此哺乳期妇女慎用,并建议停止哺乳。
歌礼药业(浙江)有限公司
86981008000028
盐酸拉维达韦是 NS5A 抑制剂,NS5A 是一种多功能蛋白,是 HCV 复制复合体的基本组成部分。盐酸拉维达韦可抑制病毒 RNA 复制。
*抗病毒活性 *
在体外复制子系统中,单一的盐酸拉维达韦对 HCV1a 和 1b 基`因型复制子细胞的 EC50分别为 0.12nM 和 0.02nM,对一系列含有 HCV 2a、3a、4a、5a、6a、7a 基因型 NS5A 基因关键片段的 HCV 1b 嵌合型复制子细胞的 EC50为 0.04-1.14 mM。在基于 HCV 复制子系统的体外联合抗 HCV 病毒研究中,盐酸拉维达韦与干扰素-a、NS3/4A 蛋白酶抑制剂、NS5B 聚合酶的核苷或非核苷抑制剂有叠加或协同效应。
耐药性
*细胞培养 *
在 HCV 1a 和 1b 复制子细胞系及一系列含有 HCV 2a、3a、4a、5a、6anS5A 基因关键片段的 HCV 1b 嵌合型复制子细胞系中,采用集落形成分析法筛选了盐酸拉维达韦的耐药变异株,基因型分析发现导致盐酸拉维达韦耐药性的突变主要是 NS5A 蛋白区域 1 的氨基酸残基 28、30、31 和 93 位点的一个或多个替代,在所有 HCV 基因亚型中含有这四个关键残基位点的替代均能增强对盐酸拉维达韦的耐药性。与 HC 1b 复制子单一氨基酸位点替代相比,HCV 1a 复制子的单一替代的耐药性更高,在 HCV2a 和 6a NS5A 氨基酸残基 28、HCV 3a NS5A 氨基酸残基 93 上的替代可产生更高水平的耐药性。
交叉耐药
盐酸拉维达韦对含有环保霉素 A 及其他类型 HCV 抑制剂(如 NS3 抑制剂、NS5B 核苷和非核苷抑制剂)耐药性替代的 HCV 1b 复制子仍具有抑制作用,与其对野生型 HCV 1b 复制子的抑制作用相当含有 L31V + Y93 H 替代的盐酸拉维达韦耐药 HCV 1a 复制子对环保霉素 A 及其他类型 HCV 抑制剂(如 NS3 抑制剂、NS5B 核苷和非核苷抑制剂)仍保持这完全的敏感性。通过其他 NS5A 抑制剂筛选出的耐药变异体,对盐酸拉维达韦也具有交叉耐药性。
遗传毒性
盐/酸拉维达韦细菌回复突变试验、体外染色体畸变试验和大鼠体内骨髓微核试验结果均为阴性。
生殖毒性
大鼠经口给予盐酸拉维达韦 750 mg/kg,未见对雌、雄大鼠生育`力和早期胚胎发育的明显影响。
妊娠大鼠于器官形成期经口给予盐酸拉维达韦 30、150 和 750 mg/kg,未见给药相关的明显畸形。但各组均可见给药相关的骨骼发育延迟现象,表现为少数骨骼(主要是顶骨、枕骨、尾骨和骶骨椎弓、以及第 9-13 胸椎)未骨化和/或骨化不完全发生率升高;此外,各组均有 1 只胎仔甲状腺缺失或较小,不能排除给药相关性。
妊娠兔于器官形成期经口给予盐酸拉维达韦 25、100 和 250 mg/kg,在 100、250 mg/kg 剂量下,母体动物可见一过性的体重减轻和摄食量减少,胚胎胎仔发育可见明显影响,包括:胚胎胎仔死亡(仅见于 250 mg/kg),多种累及椎骨的畸形以及其它骨骼畸形/变异顶间骨畸形、颈椎存在为额外骨化点)发生率剂量相关性的升高。
雌性大鼠于妊娠期第 6 天至哺乳期第 21 天经口给予盐酸拉维达韦 30、150、750 mg/kg,F0 代母鼠在 750 mg/kg 剂量下可见摄食量的一过性降低,泌乳能力、哺乳行为、生殖能力和脏器大体形态均未见给药相关的明显异常;各组 F1 代大鼠外观、存活率、离乳前后体重、生理发育、反射机能、学习行为、自发活动以及生殖功能均未见给药相关的异常。
盐酸拉维达韦可通过大鼠乳汁分泌,母鼠乳汁/血浆药物浓度比值在 1.0-2.6 之间。
致癌性:
尚未进行动物致癌性试验。
所有研究均以持续病毒学应答(SVR)为判定 HCV 治愈率的主要终点,其定义为在治疗结束后随访 12 周时 HCV RNA 低于 LLOQ*(SVR12)。
LLOQ*:中国大陆/期临床研究(CTR2060969)LLOQ 为 15IU/mL;中国台湾期临床研究(NCT3020095)LLOQ 为 12IU/mL。
在中国大陆和中国台湾分别完成了一项 II/III 临研究和一项 II 期临床研究以支持盐酸拉维达韦联合利托那韦强化的达诺瑞韦钠片和利巴韦林治疗慢性丙型病毒性肝炎基因 1b 型患者的有效性和安全性。
中国期临床研究(CTR20160969)
在采用盐酸拉维达韦片联合利托那韦强化的达诺瑞韦钠片和利巴韦林,治疗初治的慢性丙型病毒性肝炎基因 1 型患者的国内临床试验(CTR20160969)中,试验采用多中心、随机、双盲、全安慰剂平行对照的试验设计,设置了 5 周的筛选期、12 周治疗期(试验组)和 24 周治疗结束后随访期(全安慰剂对照组揭盲后接受 12 周的研究药物联合治疗。受试者为确诊为慢性丙型病毒性肝炎基因 1 型、非肝硬化且未接受过任何干扰素和/或其他直接抗病毒药物治疗的患者。治疗方案为盐酸拉维达韦片 200 mg,1 次/日;利托那韦 100 mg/达诺瑞韦钠片 100 mg,2 次/日;利巴韦林片,每次 500 mg 或 600 mg,2 次/日;疗程 12 周。主要终点为达到 SVR12 的受试者比率。
424 例受试者接受治疗,年龄从 21 岁-74 岁平均 46 岁;201 例男性约占 47.41%,223 名女性约占 52.59%。受试者平均体重为 62.28 kg 平均身高为 1.64m,平均体重指数为 23.13 kg/m2;基线时受试者体内 HCV RNA 平均水平约为 6.16log10IU/mL(约 145 万 IU/mL),所有受试者筛选时肝脏均为非肝硬化状态。所有受试者均为 HCV GT1 型感染者,其中 8 例(1.89%)为 HCV GT1a 感染者,416 例(98.11%)为 HCV GT1b 感染者。
研究结果显示,盐酸拉维达韦联合利托那韦强化的达诺瑞韦钠片和利巴韦林片治疗 12 周后,主要终点获得 SVR12 的试验组受试者比率为 95.91%(305/318,FAS)和 98.71%(305/309,PPS*)。获得 SVR12 的受试者比率的 95%CI 区间下限大于 75%(预先设定的优效界值),差异有显著统计学意义(见表 5)。
表 5:中国 II/III 期临床研究(CTR20160969)获得 SVR12 的受试者比率
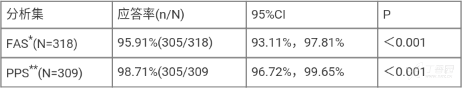
FAS:全分析数据集,所有经随机化分组,至少接受了一次治疗、且至少一次具有用药后评价数据的病例集合。
PPS**:符合方案数据集,符合纳入标准、不符合排除标准、完成治疗方案的病例集合。
本次临床研究为双盲全安慰剂对照研究,若试验组达到 SVR12 的受试者比率的 95%CI 区间下限大于 75%,则认为优效性成立。
受试者在治疗期的前 4 周体内 HCV RNA 水平均迅速下降,病毒学应答率持续升高;自治疗 4 周至治疗后随访 12 周期间,受试者的病毒学应答率为 95.91%-96.86%(见表 6)。
表 6:中国 II/III 期临床研究(CTR20160969)中病毒学应答率随时间的变化
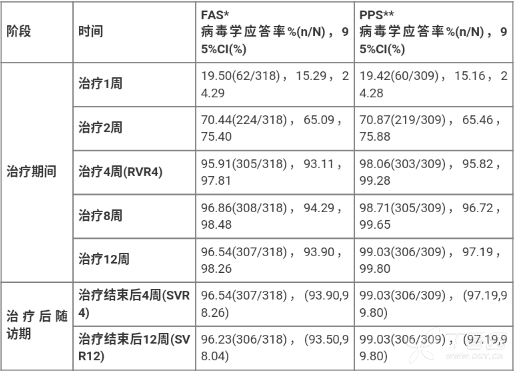
FAS:全分析数据集,所有经随机化分组,至少接受了一次治疗、且至少一次具有用药后评价数据的病例集合。
PPS**:符合方案数据集,符合纳入标准、不符合排除标准、完成治疗方案的病例集合。
治疗期间有三例受试者发生病毒学突破,没有受试者出现复发(表 7)。
*表 7:中国 II/III 期临床研究(CTR20160969)3 名受试者发生病毒学突破的分析 *
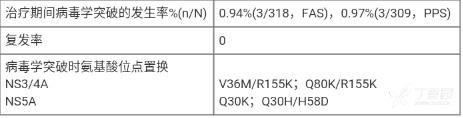
*中国台湾期临床研究(NCT03020095) * 在采用盐酸拉维达韦联合利托那韦强化的达诺瑞韦钠片和利巴韦林片,治疗初治的慢性丙型病毒性肝炎基因 1 型患者的台湾临床试验(NCT03020095)中,采用多中心、开放的单臂试验设计受试者为初治基因 1 型的非肝硬化慢性丙型肝炎患者。治疗方案为盐酸拉维达韦片 200 mg,1 次/日;利托那韦 100 mg/达诺瑞韦钠片 100 mg,2 次/;利巴韦林片,每次 500 mg 或 600 mg,2 次/日;疗程 12 周。主要终点为达到 SVR12 的受试者比率。
38 例受试者年龄从 28 岁-85 岁,平均 56.6 岁 12 例男性约占 31.6%,26 例女性约占 68.4%;平均体重为 62.44 kg,平均身高为 160.92 cm,平均体重指数为 38.0 kg/m2;基线时受试者体内 HCV RNA 平均水平约为 6.44log10U/mL(279 万 U/mL),所有受试者基线时均为无肝硬化。1 例受试者为 HCVGT1a 感染者,37 例受试 HCV 者为 GT11b 感染者。
研究结果显示,盐酸拉维达韦片联合利托那韦强化的达诺瑞韦钠片和利巴韦林片治疗 12 周后,获得 SVR12 的受试者比率为 100%(38/38,TT 和 PPS)。
受试者在治疗期的前 4 周体内 HCV RNA 水平均迅速下降,病毒学应答率持续升高;自治疗 4 周开始至治疗后 12 周期间,受试者的病毒学应答率为 73.7%100%(表 8)。
*表 8:中国台湾 1 期临床研究(NCT03020095)中病毒学应答率随时间的变化 *
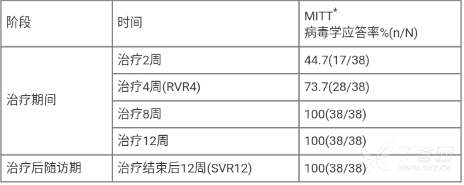
MITT*:是指所有经筛选合格入组,并且至少使用一次试验药物且至少有一次试验治疗后评价数据的受试者集合。
治疗期间无病毒学突破,治疗结束后无受试者出现复发。
健康志愿者 200 mg 单次给/药
在中国健康成年人受试者中,盐酸拉维达韦片 200 mg 单次给药后,盐酸拉维达韦的 Cmax平均值(CV%)为 3286.79 ng/mL(24.8%),AUC0-24 h平均值为 26669.27(24.9%)ngh/mL。盐酸拉维达韦 200 mg 联合利托那韦强化的达诺瑞韦钠单次给药`后,盐酸拉维达韦的 Cmax平均值(CV%)为 4124.07 ng/mL(33.9%),AUC0-24 h平均值为 46577.65.27(36.7%)ngh/mL。
健康志愿者 200 mg 连续给药
在中国健康成年人受试者中,盐酸拉维达韦片 200 mg 连续 7 天给药后,盐酸拉维达韦达稳态,盐酸拉维达韦的 Cax 几何平均值(cv%)为 4453.20 ng/ml(24.7),AUCO-24 h为 43602.93.86(39.4%)ng*h/mL,Cmin为 436.80 ng/ml(57.5%)。
患者 200 mg 单次给药
一项在美国进行的临床研究(临床试验 PPI-668-201)显示,在慢性丙型肝炎高加索人患者中,盐酸拉维达韦 200 mg(100 mg 规格胶囊 2 粒)单次给药后,盐酸拉维达韦的 Cmax几何平均值(CV%)2160 ng/mL24.5%),AUCO-12 h为 16100 ng*h/mL(34.2%)。
患者 200 mg 连续给药
一项在美国进行的临床研究(临床试验 PPL-668-201)显示,在慢性丙型肝炎高加索患者中,盐酸拉维达韦 200 mg(100 mg 规格胶囊 2 粒)连续 56 天给药,盐酸拉维达韦的 Cmax几何平均值(CV%)为 2980 ng/mL(32.4%),AUCO-12 h为 28117.399 ng*h/mL(31.62%)。
一项在美国进行的临床研究(临床试验 PP-668-201)显示,非肝硬化患者和肝硬化患者(Child-Pugh-)的暴露量没有区别。
吸收
口服给药盐酸拉维达韦片易于吸收,大约 3 小时达到血浆峰浓度。盐酸拉维达韦的 Cmax、AUC 和 Cmin以剂量比例的方式增加。每天给药一次,给药当天即可达到稳态。盐酸拉维达韦 200 mg 剂量水平在健康受试者和 hC 感染受试者之间的暴露量关系为:患者的暴露量低于健康受试者,患者的变异率高于健康受试者。
食物对口服吸收的影响
尚未进行 200 mg 盐酸拉维达韦片的食物影响研究。
一项在美国和澳大利亚进行的临床研究(PPI-668-101)中,与空腹状态给药相比,健康受试者于标准高脂肪餐(大约 50% 的热量由脂肪提供,总热量为 800-1000 卡路里)后给药盐酸拉维达韦 80 mg 胶囊,盐酸拉维达韦的 Cmax下降了 30.4%,AUC 基本未发生变化(餐后/空腹:103.4%)。
分布
稳态下,所研究剂量 10M 盐酸拉维达韦与人血浆中蛋白结合率约为 98.1%。非临床^大鼠和食蟹猴研究结果显示,盐酸拉维达韦在肝脏中浓度显著高于血浆浓度。
*代谢 * 体内和体外研究中发现,盐酸拉维达韦相当稳定,仅观察到低级程度的代谢。使用获取来自健康志愿者体内的血浆样本,检测到 3 种代谢产物,3 种代谢产物总和没有超过盐酸拉维达韦的 2% 水平。
排泄
盐酸拉维达韦片 200 mg 健康受试者单次口服给药后,半衰期约为 7.5 小时,清除率为 7.08L/h。盐酸拉维达韦片 200 mg 患者口服给药后,半衰期约为 7.4 小时,清除率为 11.1l/h。
非临床药代动力学研究表明,胆道排泄是盐酸拉维达韦已吸收剂量的主要消除途径,粪便排泄是未吸收剂量的主要消除途径。
片剂
0.2g(以C42H50N8O6计)
2272.00元
国药准字H20200008

